题目内容
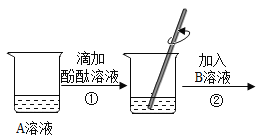
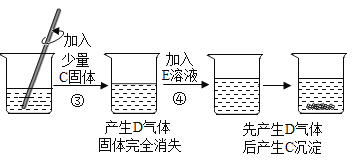
【题目】实验小组的同学研讨初中常见酸、碱、盐之间的反应关系时,做了如下实验,实验中的每一步均有明显现象,实验操作及部分现象如下图所示。
(资料)①CaCl2+Na2CO3=CaCO3↓+2NaCl ②氯化钙溶液呈中性。
回答下列问题:
(1)气体D的化学式为_____________。
(2)步骤②的实验现象为_______________。
(3)E溶液中的溶质可能是____________。
(4)B溶液的溶质由两种元素组成,④中产生气体的反应的化学方程式为______________。
(5)实验后将盛有C固体烧杯中的上清液取出少量,继续加入E溶液,仍有C固体析出,已知A与E中的阳离子相同,则实验后所得溶液含有的溶质为_____________。
【答案】CO2 红色液体变为无色 Na2CO3 Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaCl、CaCl2、酚酞
【解析】
酚酞试液遇碱性溶液变红,遇酸性溶液不变色,步骤①中有明显现象,A溶液一定呈碱性,步骤②是加入B溶液后有明显实验现象,B可能加入酸溶液,例如盐酸,该实验的实验现象是红色褪去,步骤③加入少量的固体C,产生了D气体,固体完全消失,酸和碳酸盐反应放出二氧化碳,C可能碳酸钙,D气体可能二氧化碳,溶液在存在氯化钙或氯化钙和盐酸;步骤④是加入溶液E,先产生D气体后产生C沉淀,碳酸钠加入氯化钙和盐酸混合溶液中,先与盐酸反应生成二氧化碳,再与氯化钙反应生成碳酸钙沉淀,所以E溶液是碳酸钠溶液。代入实验过程,符合题意。
根据以上分析可知:
(1)气体D是二氧化碳,其化学式为:CO2;
(3)酸性溶液能与碱性溶液反应,生成中性溶液,所以步骤②的实验现象为红色液体变为无色;
(4)E溶液中的溶质可能是Na2CO3;
(5)B溶液的溶质由两种元素组成,B可能是盐酸,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,④中产生气体的反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)实验后将盛有C固体烧杯中的上清液取出少量,继续加入E溶液,仍有C固体析出,说明有氯化钙存在,同时有生成的氯化钠和酚酞,实验后所得溶液含有的溶质为NaCl、CaCl2、酚酞。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
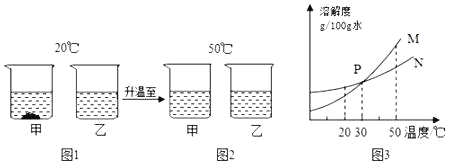
小学生10分钟应用题系列答案【题目】某化学兴趣小组同学在实验室发现了一瓶标签残缺的无色溶液(常温下,如图所示),为确认其成分,他们进行了如下探究活动。

根据标签受损的情况判断,这瓶试剂不可能是____(填“酸”、“碱” 或“盐”)。
老师提示:无色溶液可能为NaCl溶液、NaOH溶液、Na2CO3溶液和NaHCO3溶液中的一种。
(查阅资料)
四种物质的溶解度信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
(资料分析)
通过对四种物质溶解度信息的分析,这瓶无色溶液一定不是______。
(进行实验)
为了进一步确定无色溶液的成分,化学兴趣小组同学进行了实验,并记录如下。
实验组别 | 实验步骤 | 实验现象 | 实验结论 |
1 | 取无色溶液于试管中,滴加酚酞溶液 | 溶液由无色变为红色 | 无色溶液一定不是_______ |
2 | 取无色溶液于试管中,滴加稀盐酸 | 刚开始无明显现象,一会儿有气泡产生 | 无色溶液是部分变质的NaOH溶液 |
NaOH溶液暴露在空气中容易变质,反应的化学方程式为:_______。
小樊同学对实验2的结论产生了质疑,他通过查阅资料得知:碳酸钠和稀盐酸反应,当稀盐酸的量不足时会生成碳酸氢钠,足量时生成二氧化碳和水。他认为无色溶液也可能是Na2CO3溶液。于是他们又进行了如下探究活动。
实验组别 | 实验步骤 | 实验现象 | 实验结论 |
3 | 取无色溶液于试管中,滴加足量氯化钙溶液,充分反应后过滤,向滤液中滴加氯化镁溶液 | 滴加氯化钙溶液时有白色沉淀生成,过滤后向滤液中滴加氯化镁溶液无明显现象 | 无色溶液是_______ |
(释疑与反思)
碳酸钠和稀盐酸反应,稀盐酸的量不同时生成物也不同。请你再举出一个反应物的量不同时,生成物也不同的例子:________。
【题目】小明拿起家中的水壶准备煮水时,发现壶内有些褐色的固体。为了探究其成分,与兴趣小组同学查阅资料后获知这些褐色的固体是水垢,它可能是因为水中含有Ca(HCO3)2和Mg(HCO3)2等可溶性物质在加热时生成CaCO3和Mg(OH)2。
(1)含有较多Ca(HCO3)2的水称_____,加热时发生反应的化学方程式为_____。
(2)小明认为该水垢的成分只有CaCO3;但小白不同意,认为也可能只有Mg(OH)2,还可能是_____。
(3)小明为了证明自己的猜想,设计如下实验方案:
实验操作 | 现 象 | 结 论 |
①取少量水垢于试管中,加入过量的_____。 | 观察到现象_____。 | 水垢中有CaCO3 |
②向①反应后的试管中滴加2-3滴NaOH溶液 | 观察到现象_____。 | 水垢中没有Mg(OH)2,我的猜想成立 |
(3)小白不认可小明的结论,认为他的实验操作有缺陷,原因是_____。
【题目】下列方法不能达到除杂目的的是( )
选项 | 物质(括号内为杂质) | 方法 |
A | N2(O2) | 将混合气体通过灼热铜网 |
B | Fe粉(Cu粉) | 加入足量稀H2SO4充分反应,过滤,洗涤,干燥 |
C | CaO(CaCO3) | 高温煅烧 |
D | FeCl2溶液(CuCl2) | 加入足量Fe粉,充分反应后过滤 |
A.AB.BC.CD.D