题目内容
【题目】A~D为实验室中未贴标签的4种溶液,分别为:澄清石灰水、碳酸钠溶液、稀盐酸和氢氧化钠溶液.化学小组的同学们为了确定其成分,开展了探究实验.

(1)将A、B、C、D溶液两两混合,观察到的现象记录如图1所示(图中“﹣”代表无明显现象).
①物质B是__________(写化学式);
②写出A与D反应的化学方程式__________.
(2)某同学将如图2两支试管充分反应后的废液倒入同一烧杯中,观察到有气泡产生,充分反应后得到澄清溶液,则该溶液中溶质的组成可能是__________.
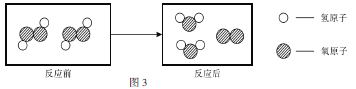
(3)利用鉴别出的盐酸,同学们又开展了实验.他们取等质量的Mg、Zn两种物质分别于等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图3所示.反应结束后一定有剩余的是__________;B反应至a点时,所得溶液中的溶质为__________(写化学式).
【答案】NaOH Na2CO3+Ca(OH)2=CaCO3↓+2NaOH NaCl、CaCl2或NaCl、CaCl2、HCl Mg ZnCl2、HCl
【解析】
(1)碳酸钠和氢氧化钙反应会生成碳酸钙沉淀,碳酸钠和盐酸反应会生成二氧化碳气体,氢氧化钠、氢氧化钙和盐酸反应,没有明显现象,所以
①D和C反应会生成气体,和A反应会生成沉淀,所以D是碳酸钠,C是盐酸,A是氢氧化钙,B是氢氧化钠,化学式为:NaOH;
②A与D的反应是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)A和C的反应是盐酸和氢氧化钙反应生成氯化钙和水,C和D的反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以将图2两支试管充分反应后的废液倒入同一个烧杯中,观察到有气泡产生,充分反应后得到澄清溶液,则该溶液中溶质的组成可能是NaCl、CaCl2或NaCl、CaCl2、HCl;
(3)A曲线的斜率大,所以A是镁,B是锌,每24份质量的镁会消耗73份质量的盐酸,每65份质量的锌会消耗73份质量的盐酸,所以取等质量的Mg、Zn两种物质分别于等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图3所示.反应结束后一定有剩余的是Mg,B反应至a点时,氢气的量没有达到最大值,所得溶液中的溶质为ZnCl2、HCl。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案