题目内容
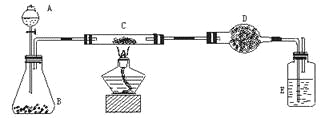
【题目】某化学兴趣小组在实验室做了如下图所示的A、B两个实验。
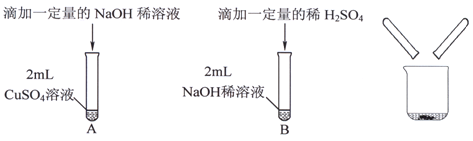
①判断实验B中是否发生反应的方法是 (13) 。
②A、B两个实验结束后,将两支试管中的物质同时倒入一洁净的烧杯中(如上图所示),混合,观察到烧杯中有蓝色沉淀,等一段时间后,同学们过滤烧杯内的物质后,对所得滤液中溶质的成分进行探究。
③【假设】假设1:滤液中的溶质是Na2SO4:
假设2:滤液中的溶质是Na2SO4、CuSO4;
假设3:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
假设4:滤液中的溶质还可能是 (14) 。
【讨论】你认为上述假设中 (15) 一定不合理,理由是 (16) ;
如果滤液为无色,还可排除的假设是 (17) 。
④【实验】某同学通过以下实验方案及现象证明假设4成立,请补充完成下表实验。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴入 (18) | (19) | 假设4正确 |
【答案】(13)在氢氧化钠溶液中滴加几滴酚酞,再滴加稀硫酸,至红色褪去(14)Na2SO4、NaOH(15)假设3(16)溶液中含有硫酸,蓝色沉淀就不可能产生(17)假设2
(18)氯化钡溶液,再滴加酚酞(19)有白色沉淀溶液变红色
【解析】
试题分析: 判断方法是在氢氧化钠溶液中滴加几滴酚酞,溶液变红,再滴加稀硫酸,至红色褪去。根据反应物的质量判断: 假设4:滤液中的溶质还可能是Na2SO4、NaOH;但是假设中如有H2SO4,则不可能有蓝色沉淀Cu(OH)2;如果滤液为无色,则不能有CuSO4,因为它为蓝色的溶液。证明假设4成立,可加氯化钡溶液,再滴加酚酞,产生有白色沉淀 溶液变红色。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目