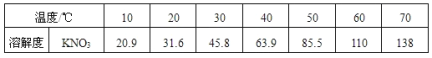
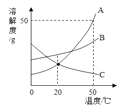
题目内容
【题目】化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验。实验装置如下图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物)。
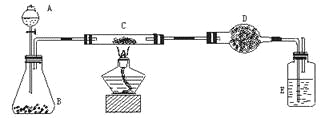
实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g。样品中铜的质量分数=[w-(b-a)×12/44]/w
请回答下列问题。
①主要实验内容
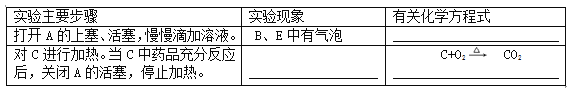
②实验讨论
装置E中盛放的试剂是 ,其作用是 。
按上述实验,得到铜的质量分数不精确,你认为是 (填:偏大、偏小、或不能确定),原因是 ,如果要得到了较正确的结果,对该装置改进的方法是 。
【答案】(12)2H2O2![]() 2H2O+O2↑(13)C中的灰红色粉末变成黑色 (14)2Cu+O2===2CuO
2H2O+O2↑(13)C中的灰红色粉末变成黑色 (14)2Cu+O2===2CuO
(15)澄清石灰水 (16)检验D装置是否完全吸收了二氧化碳 (17)偏小
(18) 水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大
(19)在装置B与C之间接一个与D相同的装置
【解析】试题分析: 滴加过氧化氢溶液,发生反应2H2O2![]() 2H2O+O2↑所以B、E中有气泡冒出,C中过量的C和生成的Cu与O2反应,即方程式为2Cu+O2===2CuO ,产生的现象为 C中的灰红色粉末变成黑色;D中盛放的是固体氢氧化钠和氧化钙的混合物,是作为干燥剂,可以吸收水蒸气和CO2;装置E中盛放的试剂是澄清石灰水,检验D装置是否完全吸收了二氧化碳;按上述实验,就会把水蒸气算成二氧化碳的质量,得到C的质量增大,Cu的质量减小导致铜的质量分数偏小;故必须要把水蒸气先干燥掉,可以在装置B与C之间接一个与D相同的装置。
2H2O+O2↑所以B、E中有气泡冒出,C中过量的C和生成的Cu与O2反应,即方程式为2Cu+O2===2CuO ,产生的现象为 C中的灰红色粉末变成黑色;D中盛放的是固体氢氧化钠和氧化钙的混合物,是作为干燥剂,可以吸收水蒸气和CO2;装置E中盛放的试剂是澄清石灰水,检验D装置是否完全吸收了二氧化碳;按上述实验,就会把水蒸气算成二氧化碳的质量,得到C的质量增大,Cu的质量减小导致铜的质量分数偏小;故必须要把水蒸气先干燥掉,可以在装置B与C之间接一个与D相同的装置。

【题目】某化学兴趣小组在实验室做了如下图所示的A、B两个实验。
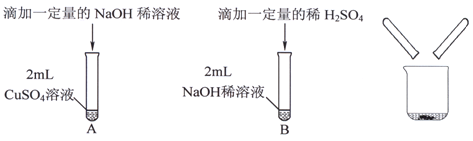
①判断实验B中是否发生反应的方法是 (13) 。
②A、B两个实验结束后,将两支试管中的物质同时倒入一洁净的烧杯中(如上图所示),混合,观察到烧杯中有蓝色沉淀,等一段时间后,同学们过滤烧杯内的物质后,对所得滤液中溶质的成分进行探究。
③【假设】假设1:滤液中的溶质是Na2SO4:
假设2:滤液中的溶质是Na2SO4、CuSO4;
假设3:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
假设4:滤液中的溶质还可能是 (14) 。
【讨论】你认为上述假设中 (15) 一定不合理,理由是 (16) ;
如果滤液为无色,还可排除的假设是 (17) 。
④【实验】某同学通过以下实验方案及现象证明假设4成立,请补充完成下表实验。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴入 (18) | (19) | 假设4正确 |