题目内容
【题目】亚硫酸盐与碳酸盐的性质相似,实验室一般采用亚硫酸钠粉末与稀硫酸反应制SO2气体。根据图示信息,回答下列问题:

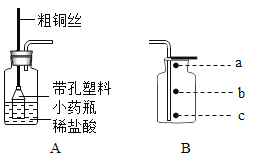
(1)图中①的仪器名称是_____。
(2)实验室制取SO2,应选择的发生装置是_____(填序号),反应的化学方程式为_____。如果直接将制SO2的发生装置与装置E相连,石蕊试纸变红,能否证明SO2能与水反应生成酸?_____(填“能”或“不能”),理由是_____。
(3)SO2对大气的影响是会引起_____,实验中可以选择装置_____进行尾气处理,你的选择理由是_____。
【答案】长颈漏斗 A或B Na2SO3+H2SO4=Na2SO4+H2O+SO2↑ 不能 需要验证干燥的二氧化硫不能使石蕊试纸变红 酸雨 G G中的漏斗使二氧化硫与氢氧化钠溶液的接触面积增大,吸收效果更好
【解析】
(1)由图可知,图中①的仪器名称是长颈漏斗,故填长颈漏斗。
(2)采用亚硫酸钠粉末与稀硫酸反应制SO2气体,是固体与液体在常温条件下反应生成气体,应选择固液常温发生装置,装置A、B均为固液常温发生装置,均可,故填A或B;
亚硫酸钠与稀硫酸反应生成硫酸钠、水和二氧化硫,故反应的化学方程式写为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;
制SO2的发生装置与装置E相连,石蕊试纸变红,不能证明SO2能与水反应生成酸,故填不能;
石蕊变红有可能是二氧化硫直接与石蕊反应使石蕊变红,需要验证干燥的二氧化硫不能使石蕊试纸变红,故填需要验证干燥的二氧化硫不能使石蕊试纸变红。
(3)二氧化硫能够与空气中的氧气和水反应生成硫酸,与雨水混合落到地面形成酸雨,故填酸雨;
实验室中常用氢氧化钠溶液来吸收多余的二氧化硫,可以选择装置G来吸收,故填G;
G中的漏斗使二氧化硫与氢氧化钠溶液的接触面积增大,吸收效果更好,故填G中的漏斗使二氧化硫与氢氧化钠溶液的接触面积增大,吸收效果更好。

 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案