题目内容
【题目】化学与生活密切相关,化学就在我们身边。
(1)下列食物中主要富含蛋白质的是_____(填序号);

(2)生石灰常用作某些食品包装中的干燥剂,它的化学式为_____
(3)野炊后用沙土盖灭火种的主要灭火原理是_____
【答案】A CaO 隔绝氧气(或空气)
【解析】
(1)肉,蛋、奶类食物中主要富含蛋白质;植物油提供的营养素是油脂;米饭提供的营养素主要是糖类;蔬菜提供的营养素主要是维生素。故选A;
(2)生石灰即氧化钙常用作某些食品包装中的干燥剂,它的化学式为CaO;
(3)燃烧是可燃物与氧气充分接触发生的发光、放热的剧烈的氧化反应。燃烧需要同时具备的三个条件:物质有可燃性、温度达可燃物的着火点、与氧气充分接触;灭火时只需要破坏一个条件即可。野炊后用沙土盖灭火种的主要灭火原理是隔绝氧气(或空气)。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动,请你和他们一起完成以下实验探究。
(提出问题)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(查阅资料) CaCl2溶液显中性
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想I :只有CaCl2;
猜想II:有______________________。
猜想Ⅲ:有CaCl2和Ca(OH)2;
猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是______________________。(用化学方程式解释)
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
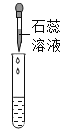
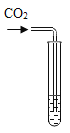
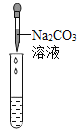
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ___________ | ___________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想III是正确的。
(评价反思)
(1) 丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____________________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑_____________________。
(反思交流)
(3) 某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如图所示,请回答下列问题:
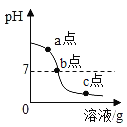
①由图可知,在c点处溶液中溶质是____________________。
②若要使c点对应的溶液变成b点对应的溶液,需要除去杂质,其中的一种方法是向烧杯中加入过量的____________________,过滤,除杂。
【题目】某化学实验小组对“影响石灰石与盐酸反应速率的因素”进行了如下探究:
(进行实验)
室温下,选用20mL不同浓度的盐酸(4%和6%)分别与1g粉末状或块状的石灰石进行实验(固定夹持仪器略去)。
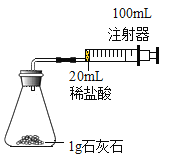
(1)按如图装置进行实验,在装药品前应检查该装置的气密性,具体方法是___________。开始实验时,应将20mL稀盐酸_______________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
(处理数据)
(2)实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 | 盐酸浓度 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳体积(mL) (均收集前30s的气体) |
a | 4% | 粉末状 | 64 |
b | 4% | 块状 | 40 |
c | 6% | 粉末状 | 98 |
d | 6% | 块状 | 65 |
①要准确比较不同形状的石灰石对反应速率的影响,可采用的方法是____________(写一种);
②从上述实验中得出的结论是颗粒越小,反应的速率越大______________。
(3)如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
气体体积/mL | 16 | 22 | 29 | 39 | 50 | 57 | 62 | 64 | 66 | 66 |
从如表数据可以分析得出,到20s后反应速率逐渐变慢,其主要原因是_____________。
(拓展延伸)
(4)比较不同形状的碳酸钙与稀盐酸反应的速率:利用如图1装置进行实验,同学们倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图2所示。
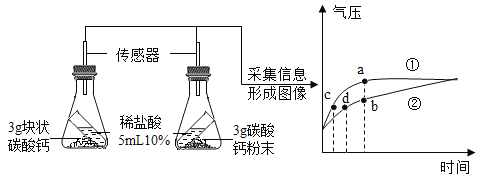
分析图象可知b点溶质______________(填化学式);c、d对比的目的___________________