ћвƒњƒЏ»Ё
°Њћвƒњ°њѕ÷”–13.4gєћће¬»їѓЄ∆—щ∆Ј£®Їђ‘”÷ ¬»їѓƒ∆£©£ђќ™ЅЋ≤вґ®—щ∆Ј÷–¬»їѓЄ∆µƒЇђЅњ£ђљЂіЋєћће»Ђ≤њ»№”Џ96.6gЋЃ÷–£ђѕтЋщµ√µƒїмЇѕ»№“Ї÷–µќЉ”“їґ®÷ ЅњЈ÷ эµƒћЉЋбƒ∆»№“Ї£ђЉ«¬ЉЅЋ»зЌЉЋщ Њµƒ«ъѕяєЎѕµ°£ћб Њ£Ї¬»їѓЄ∆”лћЉЋбƒ∆Јі”¶µƒїѓ—ІЈљ≥ћ љ£ЇCaCl2+Na2CO3 =CaCO3°э+2NaCl°£
«у£Ї£®µЏ2ќ “™«у–і≥цЉ∆Ћгєэ≥ћ£©
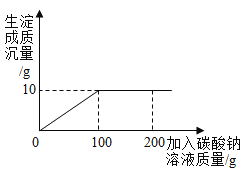
£®1£©µ±¬»їѓЄ∆”лћЉЋбƒ∆«°Ї√Ќк»ЂЈі”¶ ±£ђѕыЇƒћЉЋбƒ∆»№“Їµƒ÷ Ѕњ «_________g°£
£®2£©¬»їѓЄ∆”лћЉЋбƒ∆«°Ї√Ќк»ЂЈі”¶ЇуЋщµ√»№“Ї÷–»№÷ µƒ÷ Ѕњ «ґа…ў_______£њ
°Њір∞Є°њ100 14g
°Њљвќц°њ
£®1£©”…ЌЉ Њњ…÷™£ђЉ”»лћЉЋбƒ∆»№“Їµљ100g ±£ђ≥Ѕµн≤ї‘ў…ъ≥…£ђЋµ√чЈі”¶“—Ќк»Ђ£ђ
є ір∞Єќ™£Ї100£ї
£®2£©…и—щ∆Ј÷–¬»їѓЄ∆µƒ÷ Ѕњќ™x£ђ…ъ≥…¬»їѓƒ∆µƒ÷ Ѕњќ™y£ђ
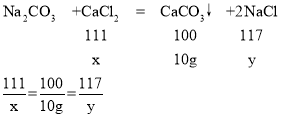
љвµ√£Їx=11.1g£ђy=11.7g£ї
—щ∆Ј÷–¬»їѓƒ∆µƒ÷ Ѕњќ™£Ї13.4g-11.1g=2.3g£ї
Ћщµ√»№“Ї÷–»№÷ ÷ Ѕњќ™£Ї 2.3g+11.7g=14g£ї
ір£ЇЋщµ√»№“Ї÷–»№÷ ÷ Ѕњќ™14g°£

 √ы–£њќћ√ѕµЅ–ір∞Є
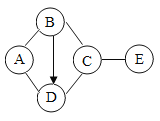
√ы–£њќћ√ѕµЅ–ір∞Є°Њћвƒњ°њ‘Џ“їґ®÷ ЅњµƒЉ„»№“Ї÷–÷рљ•Љ”»л““÷ЅєэЅњ£ђЈі”¶єэ≥ћ÷–»№“Їµƒ„№÷ Ѕњ”лЉ”»л““µƒ÷ ЅњєЎѕµ£ђƒ№”√»зЌЉ«ъѕя±н Њµƒ «£® £©
–тЇ≈ | Љ„ | ““ |
Ґў | HNO3»№“Ї | NaOH»№“Ї |
ҐЏ | HCl»№“Ї | ѓї“ ѓЈџƒ© |
Ґџ | CaCl2»№“Ї | Na2CO3»№“Ї |
Ґ№ | H2SO4»№“Ї | –њЅ£ |
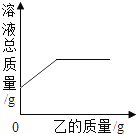
A. ҐўҐЏ B. ҐЏҐ№ C. ҐЏҐџҐ№ D. ҐўҐЏҐ№
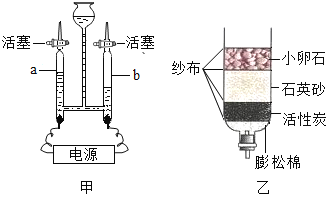
°Њћвƒњ°њѕ¬Ѕ–”–єЎ µ—йЈљ∞Є…иЉ∆’э»Јµƒ «£®°°°°£©
—°ѕо | µ—йƒњµƒ | µ—йЈљ∞Є |
A | ≥э»• | љЂєћће≥дЈ÷»№љв£ђєэ¬Ћ°Ґ’фЈҐ |
B | ≥э»• | Љ”»лєэЅњµƒ |
C | Љш±рЇф≥ц∆шћеЇЌњ’∆ш | ”√ішїр–«µƒƒЊћхЈ÷±р…м»лЉѓ∆ш∆њ÷– |
D | Љш±р»нЋЃЇЌ”≤ЋЃ | Ј÷±р»°µ»Ѕњ“Їће”Џ ‘є№÷–£ђЉ”»лµ»ЅњЈ ‘нЋЃ |
A. AB. BC. CD. D