题目内容
【题目】电荷数为1﹣18的元素的原子结构示意图等信息如图,请回答下列问题:
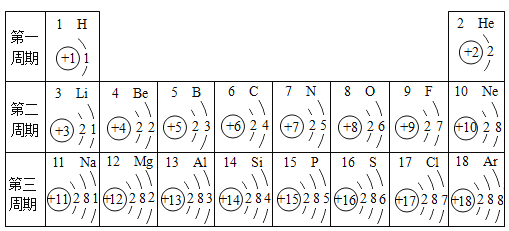
认真分析信息,回答:
(1)地壳中含量最多的元素的原子序数是_____。
(2)从Na、Mg原子结构示意图推知,金属Na、Mg化学性质不同的原因是_____。
(3)![]() 表示的粒子是_____(填粒子符号)。
表示的粒子是_____(填粒子符号)。
(4)写出一个由原子序数6、8、11的三种元素组成的化合物的化学式_____。
【答案】8 原子的最外层电子数不同 Al3+ Na2CO3
【解析】
(1)根据地壳中元素的含量来分析;
(2)根据原子结构的最外层电子数决定元素的化学性质来分析;
(3)根据微粒结构来分析;
(4)根据元素的种类以及化学式的写法来分析。
(1)地壳中含量最多的元素是氧,氧元素的原子序数是8;故填:8;
(2)从Na、Mg原子结构示意图推知,金属Na、Mg化学性质不同的原因是钠原子最外层电子数是1,镁原子最外层电子数是2,钠原子比镁原子更容易失去电子。
故填:原子的最外层电子数不同;
(3)该粒子核内有13个质子,核外有10个电子,所以是带有3个单位正电荷的铝离子;故填:Al3+;
(4)6号元素是碳元素,8号元素是氧元素,11号元素是钠元素,三种元素可以组成的化合物有碳酸钠;故填:Na2CO3。

【题目】纯碱产品中常含有少量的氯化钠杂质,在实验室中取50g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为30g),每次充分反应后都进行称量,得到的实验数据如表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入纯碱样品的质量/g | 10 | 10 | 10 | 10 | 10 |
电子天平的示数/g | 137.8 | a | 153.4 | 161.2 | 171.2 |
(1)a的值为_____。
(2)计算纯碱样品中碳酸钠的质量_____。
(3)计算所用稀盐酸的溶质质量分数_____。