题目内容
【题目】NaCl、KNO3两种固体物质的溶解度曲线如图所示。下列说法正确的是:
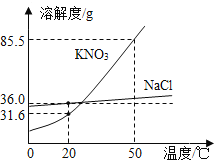
A.KNO3的溶解度大于NaCl的溶解度
B.将两种物质的饱和溶液从50℃降至20℃,析出KNO3最多
C.使NaCl从其饱和溶液中析出,最好采用蒸发溶剂的方法
D.20℃时,30gNaCl加入到50g水中充分溶解,所得溶液中NaCl的质量分数为37.5%
【答案】C
【解析】
A、 比较溶解度大小,一定要指明温度,否则无法比较,不符合题意;
B、硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,故将等质量的两种物质的饱和溶液从50℃降至20℃,析出KNO3最多,溶液质量未知,无法比较,不符合题意;
C、提纯溶解度受温度影响不大的物质,采用蒸发溶剂的方法,符合题意;
D、20℃时,NaCl的溶解度是36g,故50g水最多能溶解18gNaCl,将30gNaCl加入到50g水中,不能全部溶解,所得溶液是饱和溶液,所得溶液中NaCl的质量分数为26.5%,不符合题意。
故选C。

【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ、不稳定性
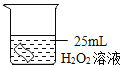
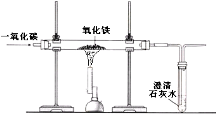
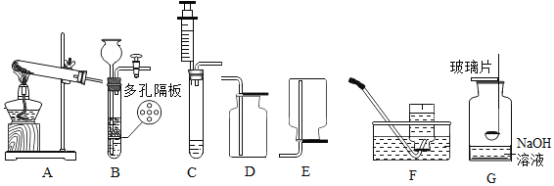
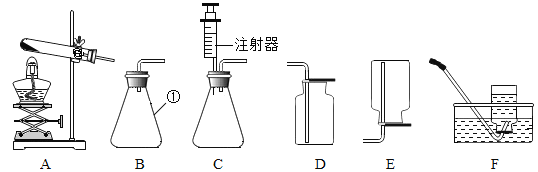
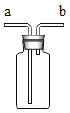
(1)如图所示进行实验,实验室用过氧化氢和二氧化锰制氧气的化学方程式为_____,属于_____反应(填反应类型)
(2)能用排水法收集O2的原因是_____。
(3)探究温度对过氧化氢分解速率的影响同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40min |
由此得出的结论是_____。
Ⅱ、腐蚀性
(査阅资料)H2O2溶液有腐蚀性。
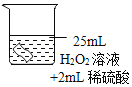
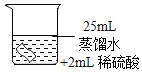
(进行实验)将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(解释与结论)
(4)实验①的作用是_____。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式:Cu+H2O2+H2SO4=CuSO4+_____。
(反思交流)
(6)某同学提出,实验②中,除发生(5)的反应外。还发生了一个反应导致有细小气泡产生,该反应的反应物为_____。
【题目】小明同学发现上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶是否变质,小明邀约几个喜欢探究的同学对此进行了探究。请你一起完成下列实验报告。
(1)(提出问题1)该溶液是否变质?
(实验探究1)
实验步骤 | 实验现象 | 解释与结论 |
取少量该溶液放于试管中,滴加足量稀盐酸 | 有__产生 | 说明该溶液已变质,变质的原因是__(请用化学方程式表示) |
(2)(提出问题2)该溶液变质程度怎样?
(提出猜想)
猜想一:已完全变质,该溶液中溶质只含Na2CO3
猜想二:部分变质,该溶液中溶质含有NaOH和Na2CO3。
(查阅资料)氯化钡溶液呈中性。
(实验探究2)
实验步骤 | 实验现象 | 结论 |
先取少量该溶液放于试管中,加入过量氯化钡溶液 | 有__生成 | 猜想__成立 |
静置,取上层清液于另一支试管中,加入2﹣3滴酚酞溶液 | 上层清液变红 |
(3)(提出问题3)
怎样提纯该样品得到纯净的氢氧化钠固体。
(实验探究3)
为得到纯净的氢氧化钠固体,同学们取该样品并设计了如下实验方案。请回答下列问题:试剂X可以选用___的溶液(写出溶质化学式),操作a和操作b中都需要用到玻璃棒,其中操作a中玻璃棒的作用为__。
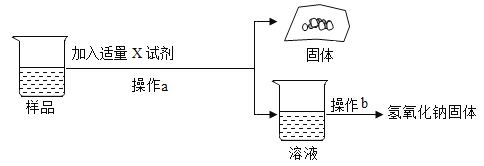
(4)(反思交流)在(实验探究2)中加入过量的氯化钡溶液的目的是什么__?
【题目】某研究小组在学习氧气的化学性质时发现:铁丝、木炭燃烧没有火焰,蜡烛(主要成分是石蜡)燃烧却有明亮的火焰.该小组同学进行了如下探究.
(1)写出蜡烛燃烧的文字表达式:______.
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示).由此可知:蜡烛燃烧产生的火焰是由___(填“固态”或“气态”)物质燃烧形成的.

物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50至70 | 300至550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
(3)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
由该表可知:物质燃烧能否产生火焰与其__(填“熔点”或“沸点”)和燃烧时温度有关.通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰,由此推测:钠在燃烧时,__(填“有”或“没有”)火焰产生.
(4)根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点___硫燃烧时的温度(填“>”或“<”或“=”) .
【题目】某兴趣小组在实验室用金属和酸反应来比较铝和锌的金属活动性大小,他们将一块铝片和一块相同质量的锌粒分别放入相同浓度的稀硫酸和稀盐酸中,发现开始时锌粒产生的气体更快,对照金属活动性顺序表,铝排在锌的前面,应该铝更快,为什么会出现这种情况呢?请你一起参与以下探究。
[提出问题]除了“金属活动性、溶液的质量、溶质质量分数”外,还有哪些因素会造成锌比铝产生气体快?
[猜想与假设]猜想1:锌与铝表面的氧化物;
猜想2:酸的种类;
猜想3:温度
[实验探究] (1)按题中开始时小组同学设计的实验方案比较锌、铝的金属活动性是____________(填“合理”或“不合理” )的,原因是_______________________。
(2)请写出铝与稀盐酸反应的化学方程式_______________________。
(3)某同学设计如下实验方案进行实验:
实验步骤 | 实验现象 | 实验结论 |
取表面积相同的锌、铝,分别放入温度相同、浓度相同、体积相同的稀盐酸中 | 锌产生气体快,铝刚开始反应比锌慢,后逐渐快起来 | 猜想1__________( 填“成立"或“不成立”) |
产生这种现象的原因是______________,所以做金属与酸的反应实验时,必要的处理是___________。
[实验拓展]再写一种影响铝与酸反应快慢的因素__________________ (与以上题中提到的影响因素不同),设计合理的实验方案,并写出“实验步骤、现象和结论”。