题目内容
【题目】小明同学发现上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶是否变质,小明邀约几个喜欢探究的同学对此进行了探究。请你一起完成下列实验报告。
(1)(提出问题1)该溶液是否变质?
(实验探究1)
实验步骤 | 实验现象 | 解释与结论 |
取少量该溶液放于试管中,滴加足量稀盐酸 | 有__产生 | 说明该溶液已变质,变质的原因是__(请用化学方程式表示) |
(2)(提出问题2)该溶液变质程度怎样?
(提出猜想)
猜想一:已完全变质,该溶液中溶质只含Na2CO3
猜想二:部分变质,该溶液中溶质含有NaOH和Na2CO3。
(查阅资料)氯化钡溶液呈中性。
(实验探究2)
实验步骤 | 实验现象 | 结论 |
先取少量该溶液放于试管中,加入过量氯化钡溶液 | 有__生成 | 猜想__成立 |
静置,取上层清液于另一支试管中,加入2﹣3滴酚酞溶液 | 上层清液变红 |
(3)(提出问题3)
怎样提纯该样品得到纯净的氢氧化钠固体。
(实验探究3)
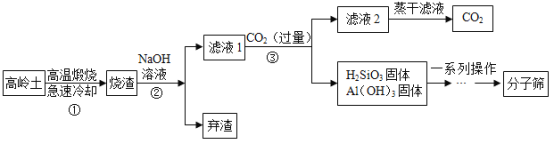
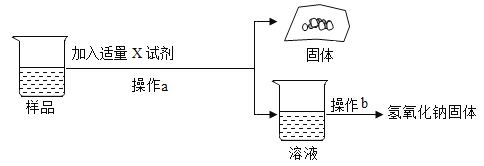
为得到纯净的氢氧化钠固体,同学们取该样品并设计了如下实验方案。请回答下列问题:试剂X可以选用___的溶液(写出溶质化学式),操作a和操作b中都需要用到玻璃棒,其中操作a中玻璃棒的作用为__。
(4)(反思交流)在(实验探究2)中加入过量的氯化钡溶液的目的是什么__?
【答案】气泡 ![]() 白色沉淀 二 Ca(OH)2 引流 将碳酸钠完全除去。
白色沉淀 二 Ca(OH)2 引流 将碳酸钠完全除去。
【解析】
氢氧化钠易与空气中二氧化碳反应生成了碳酸钠,从而变质。
(1)提出问题1:
结论为该溶液已经变质,氢氧化钠易与空气中的二氧化碳反应生成碳酸钠和水,从而变质,该反应的化学方程式为:![]() ,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,故实验现象为:有气泡产生;
,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,故实验现象为:有气泡产生;
(2)提出问题2:
实验探究2:要探究溶液中是否含有氢氧化钠,应将碳酸钠除干净,所以先取少量该溶液放于试管中,加入过量氯化钡溶液,氯化钡能与碳酸钠反应生成碳酸钡和氯化钠,实验现象为:有白色沉淀生成,可验证碳酸钠的存在,并将碳酸钠除尽,静置,取上层清液于另一支试管中,加入2﹣3滴酚酞溶液,无色酚酞试液遇碱变红,上层清液变红,说明溶液显碱性,故含有氢氧化钠,由此可知,猜想二成立。
实验探究3:该实验的目的是得到纯净的氢氧化钠,由图可知,加入试剂X后,产生沉淀,过滤,得到氢氧化钠,氢氧化钙能与碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,故试剂X可以选用氢氧化钙溶液,溶质的化学式为Ca(OH)2;
操作a和操作b中都需用到玻璃棒,其中操作a能将固液分开,操作是过滤,玻璃棒的作用为引流;
(4)反思交流:
在实验探究2中探究是否含有氢氧化钠,应将碳酸钠除去,碳酸钠能与氯化钡反应生成碳酸钡和氯化钠,所以加入过量的氯化钡溶液的目的是将碳酸钠完全除去。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】化学与生活息息相关,下列描述全部正确的一组( )
A化学与生活 | B化学与健康 |
生活中用洗洁精清洗油污的原理是乳化作用 实验室用品尝味道的方法区分食盐与白糖 | 老年人缺钙易得骨质疏松症 人体缺乏维生素A易得夜盲症 |
C化学与材料 | D化学与环境 |
塑料、天然橡胶、合成纤维都属于合成材料 玻璃钢、生铁、硬铝都属于合金 | 温室效应的形成主要与CO、CH4有关 酸雨形成主要与SO2、氮氧化合物有关 |
A. AB. BC. CD. D