题目内容
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是( )
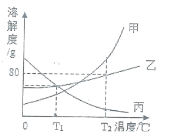
A.T2°C时, 乙的溶解度为80
B.甲中混有少量的乙,提纯甲的常用方法是蒸发结晶
C.在T1°C时,将接近饱和的丙溶液变为饱和溶液,溶液的质量一定改变
D.将T2°C的甲、 乙、丙饱和溶液温度降至T1°C,溶液中溶质的质量分数大小关系为乙=丙>甲
【答案】C
【解析】
由甲、乙、丙三种固体物质的溶解度曲线图可知,甲物质的溶解度随温度的升高而增大,乙物质的溶解度受温度的影响较小,丙物质的溶解度随温度的升高而减小。
A、由溶解度曲线图可知,T2°C时, 乙的溶解度为80g,故A不正确;
B、甲物质的溶解度随温度的升高而增大,且甲的溶解度受温度影响较大,乙物质的溶解度受温度的影响较小,甲中混有少量的乙,提纯甲的常用方法是降温结晶,故B不正确;
C、丙物质的溶解度随温度的升高而减小,在T1°C时,将接近饱和的丙溶液变为饱和溶液,可采取加入溶质或恒温蒸发溶剂的方法,加入溶质,溶液质量增加,恒温蒸发溶剂,溶液质量减小,溶液的质量一定改变,故C正确;
D、甲物质的溶解度随温度的升高而增大,乙物质的溶解度受温度的影响较小,丙物质的溶解度随温度的升高而减小,T1°C时,甲、 乙、丙的溶解度关系为乙=丙>甲,将T2°C的甲、 乙、丙饱和溶液温度降至T1°C,甲物质的溶液有晶体析出,乙有少量固体析出,丙的溶解度增加,故甲、乙还是饱和溶液,丙变为不饱和溶液,降温后,丙的溶质质量分数不变,由于T1°C时,乙的溶解度大于甲的溶解度大于T2°C时丙的溶解度,故降温后溶液中溶质的质量分数大小关系为乙>甲>丙,故D不正确。
故选C。

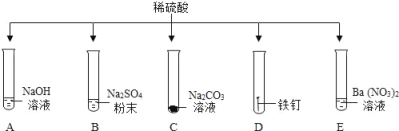
【题目】某实验小组为确定一瓶久置的碱石灰![]() 生石灰和氢氧化钠固体的混合物
生石灰和氢氧化钠固体的混合物![]() 样品的成分,进行了如下实验:取少量碱石灰样品于烧杯中,向其中加入足量水,充分溶解后,过滤,得到固体A和溶液B,并对固体A和溶液B的成分展开了探究活动。
样品的成分,进行了如下实验:取少量碱石灰样品于烧杯中,向其中加入足量水,充分溶解后,过滤,得到固体A和溶液B,并对固体A和溶液B的成分展开了探究活动。
探宄活动一:固体A的成分是什么?
(实验验证)取一定量固体A于试管中,滴加稀盐酸,有气泡产生。固体A中一定含有______![]() 填化学式
填化学式![]() 。
。
探究活动二:探究溶液B中溶质成分是什么?
(猜想与假设)猜想①; NaOH;猜想②:![]() ;猜想③:NaOH和
;猜想③:NaOH和![]() ;猜想④:NaOH和______。
;猜想④:NaOH和______。
(实验探究)小明、小强同学分别进行如下实验并得出相应的结论:
小明同学:取少量溶液B于试管中,滴加几滴酚酞溶液,溶液变成红色,则溶液B中溶质一定含有NaOH。
小强同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中溶质是![]() 。
。
(反思与评价)同学们认真分析上述两位同学的实验,认为他们的结论均有不足之处,不能确定溶液B中溶质的成分,请指出小明同学结论的不足之处是______。为进一步确认溶液B中溶质的成分,同学们继续做了如下实验。
实验步骤 | 实验现象 | 实验结论 |
步骤Ⅰ:取少量溶液B于试管中,加入 ______ | 有白色沉淀生成 | 猜想③正确 |
步骤Ⅱ:取步骤Ⅰ中上层清液少许于试管中,向其中滴加硝酸铜溶液。 | ______ |
(反思与拓展)
实验过程中,同学们发现向样品中加水时还放出大量的热。综合以上探究,下列对碱石灰样品成分分析正确的是______![]() 填字母序号
填字母序号![]() 。
。
A 一定含有NaOH
B 一定含有![]()
C 一定含有CaO
D 至少含有NaOH、CaO中的一种
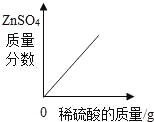
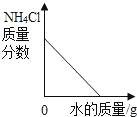
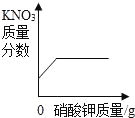
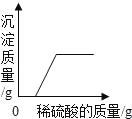
【题目】下列图象与所述实验相符的是( )
A | B | C | D |
向一定量锌粒中加入过量稀硫酸 | 向一定量氯化铵饱和溶液中不断加入水 | t℃时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体 | 向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸 |
|
|
|
|
A. AB. BC. CD. D