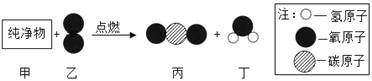
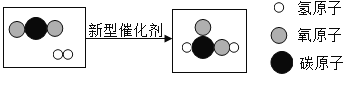
题目内容
【题目】现有混合均匀的锌银粉末,某化学兴趣小组为了测定其组成,取30g样品于烧杯中,向其中分3次加入溶质质量分数相同的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 20 | 23.5 |
第2次 | 40 | 13.5 |
第3次 | 10 | m |
试回答下列问题:
(1)上述表格中m的值为_____;
(2)该金属粉末中锌的质量分数是多少_____?
(3)所用稀硫酸中硫酸的质量分数是多少_____?
【答案】13.5 55% 49%
【解析】
由题意,取30g样品于烧杯中,向其中分3次加入溶质质量分数相同的稀硫酸,使之充分反应。第1次加入20g稀硫酸,硫酸完全反应,参加反应的锌的质量为30g-23.5g=6.5g,第2次加入40g稀硫酸,硫酸完全反应,理论上参加反应的锌的质量为![]() ,实际参加
,实际参加
反应的锌的质量为23.5g-13.5g=10g,说明第2次加入的硫酸有剩余,故第3次加入10g稀硫酸,固体不参与反应,剩余固体的质量为13.5g。
(1)由分析可知,上述表格中m的值为13.5;
(2)该金属粉末中锌的质量为30g-13.5g=16.5g,则锌的质量分数是![]() ;
;
(3)第1次加入20g稀硫酸,硫酸完全反应,参加反应的锌的质量为6.5g,设参加反应的硫酸的质量为x,则有:
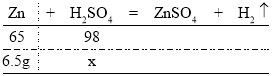
由![]() 解得x=9.8g
解得x=9.8g
所用稀硫酸中硫酸的质量分数为![]()
答:所用稀硫酸中硫酸的质量分数为49%。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目