题目内容
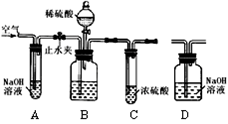
(10分)某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20 g大理石中(其它成分不与盐酸反应),把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
试回答下列问题:
(1)请在右边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;
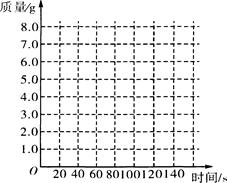
(2)从表中可以看出,20 g大理石样品与盐酸反应生成的CO2质量最多是 g;
(3)计算大理石样品中碳酸钙的质量分数。
| 时间/s | O | 20 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | O | 3.O | 5.O | 6.O | 6.6 | 6.6 | 6.6 |
试回答下列问题:
(1)请在右边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;

(2)从表中可以看出,20 g大理石样品与盐酸反应生成的CO2质量最多是 g;
(3)计算大理石样品中碳酸钙的质量分数。
(1)

(2)6.6 (3)75%。

(2)6.6 (3)75%。
(1)如右图(曲线从原点开始,80s时达到最大值6.6,此后呈水平线)曲线关系图如下

(2)由表格知当二氧化碳质量达到6.6g时质量不再增加,也就是二氧化碳的最大量是6.6g,故答案为:6.6
(3)利用已知的二氧化碳的质量,求出碳酸钙的质量.
解:设样品中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 6.6g
100:44=x:6.6g
x=15g
大理石样品中CaCO3的质量分数为:15g/20g×100%=75%
答:大理石样品中CaCO3的质量分数为75%.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目