题目内容
【题目】某同学用如图总结NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。
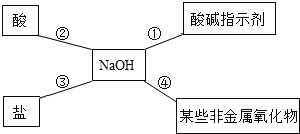
(1)为验证性质①,该同学将无色酚酞试液滴入NaOH溶液中,溶液颜色由无色变成_______________。
(2)性质②的反应为______________反应(非基本反应类型),试写出NaOH与盐酸反应的化学方程式_______________。
(3)为了验证性质③,该同学可选择的物质是_______________(填序号)
A Na2CO3 B CO2 C FeCl3 D Ba (NO3) 2
(4)写出NaOH溶液吸收CO2的化学方程式_______________。
【答案】红色 中和 ![]() C
C ![]()
【解析】
(1)氢氧化钠溶液显碱性,无色酚酞溶液遇碱变红,故该同学将无色酚酞试液滴入NaOH溶液中,溶液颜色由无色变成红色;
(2)酸与碱作用生成盐和水的反应,叫做中和反应,故性质②的反应为中和反应(非基本反应类型), NaOH与盐酸反应生成氯化钠和水,反应的化学方程式为![]() ;
;
(3)氢氧化钠不能与碳酸钠、硝酸钡反应,二氧化碳不是盐,氢氧化钠与氯化铁反应生成氢氧化铁的沉淀和氯化钠,故选C;
(4) NaOH与CO2反应生成碳酸钠和水,反应的化学方程式为![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】实验室有一瓶标签模糊的氢氧化钠溶液,为了测定其溶质质量分数,小明进行了如下实验:①取一洁净的锥形瓶称量,然后往其中加入一定量的氢氧化钠溶液,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中加入溶质质量分数为7.3%的盐酸,边加边振荡,溶液红色褪去时,再次称量。数据如下表:回答下列问题:
锥形瓶/g | 锥形瓶+氢氧化钠溶液/g | 锥形瓶+反应后溶液/g | |
质量/g | 35.5 | 60.5 | 110.5 |
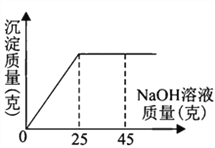
(1)根据表中数据,通过计算确定该瓶氢氧化钠溶液的溶质质量分数_________。
(2)小建用pH试纸测得小明实验反应后锥形瓶内溶液的pH为4,则小明测出氢氧化钠溶液的质量分数比实际浓度_________(选填“偏大”或“偏小”),造成这一偏差的原因是________。