题目内容
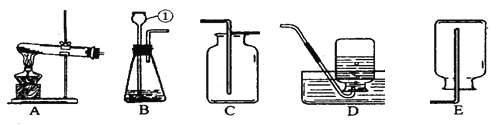
【题目】下图为初中化学常见的仪器装置,请回答下列问题。
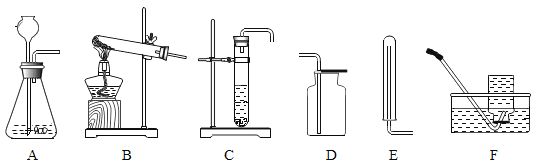
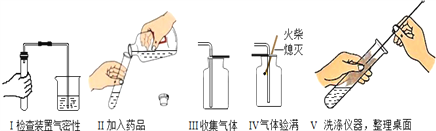
(1)实验室用KMnO4粉末制取O2的化学方程式为._____此反应所属的基本反应类型是._____;发生装置中符在试管口放一团棉花,以防止KMnO4粉末_____.
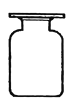
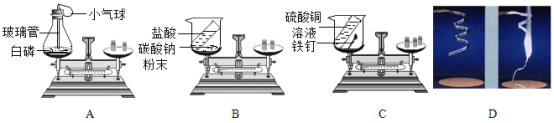
(2)实验室用双氧水和二氧化锰制取氧气,该反应的化学方程式是_____.,若需收集一瓶氧气用于铁丝燃烧的实验,应选择的发生与收集装置的组合是_____ (填字母),收集完毕,用玻璃片的_____(填"光滑面“或"磨砂面")盖住集气瓶口。
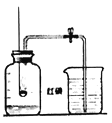
(3)用A装置制取气体时,长颈漏斗的下端管口插入液面以下.目的是_____.
(4)某同学用B装置制备氧气,实验结束时,发现试管已破裂请你帮他分析.其原因可能是_____(写一点原因即可)。
(5)某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 23.4 | 16.4 | 16.4 |
请计算:
①共制得氧气_____g
②计算反应前加入的二氧化锰的质量_____。
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 堵塞导管 2H2O2
K2MnO4+MnO2+O2↑ 分解反应 堵塞导管 2H2O2![]() 2H2O+O2↑ AF或CF 磨砂面 防止生成的气体逸出 实验结束先熄灭酒精灯(合理均可) 9.6 1.5g
2H2O+O2↑ AF或CF 磨砂面 防止生成的气体逸出 实验结束先熄灭酒精灯(合理均可) 9.6 1.5g
【解析】
(1)实验室用KMnO4粉末制取O2的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑,该反应符合分解反应一变多的特征;发生装置中需在试管口放一团棉花,以防止加热时KMnO4粉末进入导管,堵塞导管。
K2MnO4+MnO2+O2↑,该反应符合分解反应一变多的特征;发生装置中需在试管口放一团棉花,以防止加热时KMnO4粉末进入导管,堵塞导管。
故填:2KMnO4![]() K2MnO4+MnO2+O2↑;分解反应;堵塞导管。
K2MnO4+MnO2+O2↑;分解反应;堵塞导管。
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;若需收集一瓶氧气用于铁丝燃烧的实验,这个实验对氧气的纯度要求高,用排水法收集,应选择的发生与收集装置的组合是AF或CF;防止氧气从集气瓶中逸出,收集完毕,用玻璃片的磨砂面盖住集气瓶口;
2H2O+O2↑;若需收集一瓶氧气用于铁丝燃烧的实验,这个实验对氧气的纯度要求高,用排水法收集,应选择的发生与收集装置的组合是AF或CF;防止氧气从集气瓶中逸出,收集完毕,用玻璃片的磨砂面盖住集气瓶口;
故填:2H2O2![]() 2H2O+O2↑;AF或CF;磨砂面;
2H2O+O2↑;AF或CF;磨砂面;
(3)用A装置制取气体时,长颈漏斗的下端管口要伸入液面以下目的是防止生成的气体逸出;故填:防止生成的气体逸出;
(4)在实验室里用加热高锰酸钾的方法制取氧气,实验结束时发现试管破裂的可能原因是实验结束先熄灭酒精灯,导致水槽内的水倒流进试管引起试管炸裂,故填:实验结束先熄灭酒精灯;
(5)①该反应共制得氧气的质量为:26.0g-16.4g=9.6g;
②设生成氯化钾的质量为x,
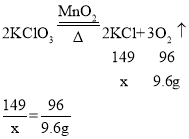
x=14.9g
故反应前加入的二氧化锰的质量为:16.4g-14.9g=1.5g。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。
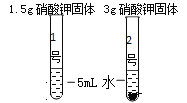
(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。由此获得的实验结论是____________。要使2号试管中的固体全部溶解,可采取的方法有___________、_____________。
(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下。请根据数据进行分析。
实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
水的质量(g) | 100 | 100 | 100 | 100 |
加入硝酸钾的质量(g) | 80 | 100 | 120 | 140 |
溶液质量(g) | 180 | 200 | 210 | M |
(1)请计算实验2中硝酸钾的溶质质量分数是_____________。
(2)现将实验2中的溶液稀释成20%的硝酸钾溶液,需要加水的质量为___________g。
(3)请判断实验2中硝酸钾溶液是________溶液。(选填“饱和”或“不饱和”)。
(4)实验4中M的数值是_______。