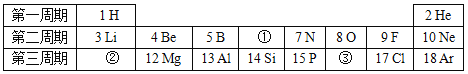
题目内容
【题目】实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。
(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。由此获得的实验结论是____________。要使2号试管中的固体全部溶解,可采取的方法有___________、_____________。
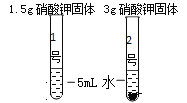
(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下。请根据数据进行分析。
实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
水的质量(g) | 100 | 100 | 100 | 100 |
加入硝酸钾的质量(g) | 80 | 100 | 120 | 140 |
溶液质量(g) | 180 | 200 | 210 | M |
(1)请计算实验2中硝酸钾的溶质质量分数是_____________。
(2)现将实验2中的溶液稀释成20%的硝酸钾溶液,需要加水的质量为___________g。
(3)请判断实验2中硝酸钾溶液是________溶液。(选填“饱和”或“不饱和”)。
(4)实验4中M的数值是_______。
【答案】一定温度下5mL水最少能够溶解1.5g硝酸钾,2号试管溶液达到饱和状态,1号试管溶液可能饱和 加水 升高温度 50% 300 不饱和 210
【解析】
[定性研究]
由此获得的实验结论是一定温度下5mL水至少能够溶解1.5g硝酸钾,2号试管溶液达到饱和状态,1号试管可能饱和可能不饱和;
硝酸钾的溶解度随温度的升高而增大,所以要使2号试管中的固体全部溶解,可采取的方法有升高温度、加水。
[定量研究]
(1)实验2中硝酸钾的溶质质量分数是:![]()
(2)设需要加水的质量为x,
根据题意有:![]()
x=300g
需要加水的质量为300g。
(3)由实验3中可知,100g水中最多溶解110g硝酸钾,实验2中硝酸钾溶液是不饱和溶液。
(4)由实验3中可知,100g水中最多溶解110g硝酸钾,实验4中M的数值是210。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案【题目】下图为初中化学常见的仪器装置,请回答下列问题。
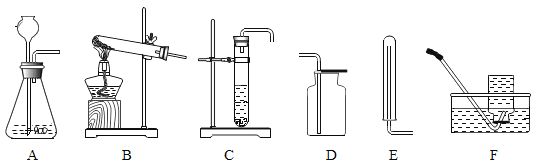
(1)实验室用KMnO4粉末制取O2的化学方程式为._____此反应所属的基本反应类型是._____;发生装置中符在试管口放一团棉花,以防止KMnO4粉末_____.
(2)实验室用双氧水和二氧化锰制取氧气,该反应的化学方程式是_____.,若需收集一瓶氧气用于铁丝燃烧的实验,应选择的发生与收集装置的组合是_____ (填字母),收集完毕,用玻璃片的_____(填"光滑面“或"磨砂面")盖住集气瓶口。
(3)用A装置制取气体时,长颈漏斗的下端管口插入液面以下.目的是_____.
(4)某同学用B装置制备氧气,实验结束时,发现试管已破裂请你帮他分析.其原因可能是_____(写一点原因即可)。
(5)某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。
加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 23.4 | 16.4 | 16.4 |
请计算:
①共制得氧气_____g
②计算反应前加入的二氧化锰的质量_____。
【题目】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用。
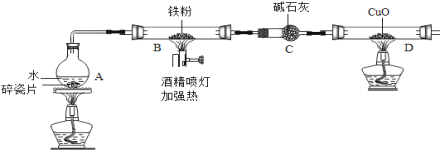
(1)(推断)观察到D中黑色固体变红,则B中生成的气体是_____;
(2)探究B装置中剩余固体成分是什么?
(查阅资料)
(1)碎瓦片能防爆沸,碱石灰是氧化钙和氢氧化钠的混合物
(2)铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引。
(3)Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(初步探究)B装置中剩余固体为黑色,能全部被磁铁吸引;
(猜想与假设)猜想一:剩余固体是Fe3O4
猜想二:剩余固体是_____;
(实验探究)请你设计实验,证实你的猜想
实验操作 | 实验现象及结论 |
_____ | _____ |
(实验结论)铁与水蒸气反应的化学方程式为_____,在该反应中,铁与水蒸气恰好反应的质量比为_____。