题目内容
【题目】某化学兴趣小组设计利用稀硫酸浸取某废弃的氧化铜锌矿制取活性氧化锌的方案(氧化铜锌矿主要成分为CuO和 ZnO,其余成分既不与酸反应,也不溶于水),部分实验流程如下:

(1)将氧化铜锌矿粉碎的目的是_________,操作 1 的名称是_____,所用到的 玻璃仪器由玻璃棒、烧杯、_____;
(2)在氧化铜锌矿中加入稀硫酸要过量,其目的是_____,主要成分发生反应的化学方程式为______________________________________ (写出一个即可);
(3)得到滤渣 1 含有的金属是___________________________________________ 。
【答案】 增大反应接触面积,使反应更充分 过滤 漏斗 使氧化铜、氧化锌充分反应 CuO+H2SO4=CuSO4+H2O (或 ZnO+H2SO4=ZnSO4+H2O) Fe 和 Cu
【解析】(1)在该实验操作中,将氧化铜锌矿粉碎的目的是增大反应接触面积,使反应更充分,操作 1 是固液分离的过程,故操作 1的名称是过滤,所用到的 玻璃仪器有玻璃棒、烧杯、漏斗;
(2)在氧化铜锌矿中加入稀硫酸要过量,其目的是使氧化铜、氧化锌充分反应 ;氧化铜与稀硫酸反应生成硫酸铜和水,反应方程式为CuO+H2SO4=CuSO4+H2O ;
(3)锌比铁活泼,铁比铜活泼,故铁可以将硫酸铜中的铜置换出来,故滤渣中有生成的铜和过量的铁。

【题目】水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指_____ (填“单质、元素、分子或原子”)。
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(Ⅰ)检验某地下水是硬水还是软水,可用的物质是_____;实验室常用_____的方法来降低水的硬度
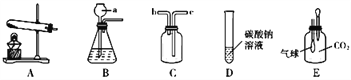
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
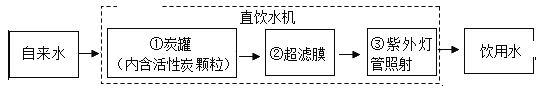
①对应的作用是_____(填字母序号)③对应的作用是_____。
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有_____。
A.工业废水直接排放 B.工业废气处理后排放
C.禁止使用含磷洗衣粉 D.大量使用化肥、农药