题目内容
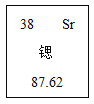
【题目】锶是一种特殊的金属,与钙的化学性质相似但比钙活泼,如图是元素周期表中“类钙”元素锶的相关信息。碳酸锶(SrCO3)可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO3和NaCl固体混合物中SrCO3的质量分数,在三个烧杯中进行相关实验,实验所用稀盐酸的溶质的质量分数相同。所得数据如下表所示:
烧杯编号 | ① | ② | ③ |
稀盐酸质量/g | 100 | 200 | 300 |
固体混合物质量/g | 100 | 100 | 100 |
反应后烧杯中物质的质量/g | 195.6 | 291.2 | 391.2 |
试求:
(1)锶原子质子数为_____,写出锶离子的符号_____。
(2)请写出碳酸锶(SrCO3)与稀盐酸反应的化学方程式_____。
(3)烧杯②中产生CO2的质量为_____g。
(4)请计算原固体混合物中SrCO3的质量分数(SrCO3的相对分子质量是148,计算结果精确到0.1%)。
【答案】(1)38,Sr2+;(2)SrCO3+2HCl=SrCl2+CO2↑+H2O;(3)8.8;(4)29.6%
【解析】
(1)由锶的元素周期表信息可知,锶元素的原子序数为38,因为原子中原子序数=质子数,所以锶原子质子数为38;根据题中提供的信息,“类钙”元素锶与钙的化学性质相似但比钙活泼,结合碳酸锶的化学式SrCO3分析,在化合物中锶元素显+2价,所以每个锶离子带2个单位的正电荷,离子符号为:Sr2+;
(2)碳酸锶(SrCO3)与稀盐酸反应生成氯化锶、二氧化碳和水,其化学方程式为:SrCO3+2HCl=SrCl2+CO2↑+H2O;
(3)由表格中的数据以及质量守恒定律可知,烧杯②中产生CO2的质量为:200g+100g-291.2g=8.8g;
(4)根据题中表格提供的数据,加入200g盐酸产生气体为:200g+100g-291.2g=8.8g,加入300g盐酸生成气体质量是:300g+100g-391.2g=8.8g,说明第二组固体已经完全反应。
设原固体混合物中SrCO3的质量分数为x
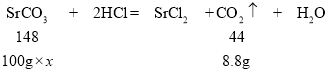
![]()
解得x≈29.6%
答:原固体混合物中SrCO3的质量分数约为29.6%。

【题目】 2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到了具有极好的抗冲击性和防潮性的HDPE膜。某化学兴趣小组对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
[提出问题] HDPE膜由什么元素组成?
[查阅资料]①HDPE膜能够燃烧,燃烧可能生成一氧化碳: ②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
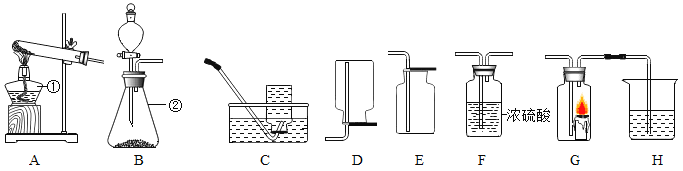
[实验探究]如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定 质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
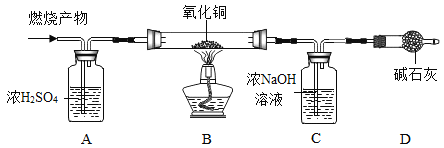
[实验记录]
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
[实验分析]
(1)实验前,先通入氮气的目的是___________________。
(2)装置A中浓硫酸的作用是___________________。
(3)实验中观察到装置B中黑色粉末变成红色,证明燃烧产物中有__________________(填化学式)。
(4)装置D的作用是___________________。
[数据处理] 4.2g的HDPE膜样品中含碳元素的质量为__________________g,含氢元素的质量为_________g。
[实验结论] HDPE膜由__________________元素组成。
[反思拓展]实验中的4.2g HDPE膜样品燃烧消耗的氧气质量为m,则m的取值范围为___________________。