题目内容
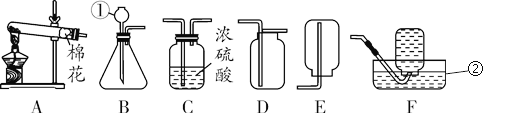
【题目】化学是一门以实验为基础的学科。根据下图回答问题:

(1)仪器①的名称是______________。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为___________________,要收集一瓶较纯净的气体,选用的发生和收集装置是______(填字母序号,下同)。
(3)实验室制取二氧化碳,发生装置要能达到“控制反应速度”,需要选用的仪器和用品有_________;反应的化学方程式为__________;选用的收集装置是C,则二氧化碳从____(填导管的序号)进入。
(4)装置H中,向干燥石蕊试纸的a端滴入蒸馏水,观察到的实验现象为_______,该实验得出的结论为___________。
(5)小明同学以废弃的“棒棒冰”塑料管为材料,制成的气体发生装置(各部分连接紧密后,如下图所示)。该实验设计的优点有:能控制反应速率和____________。(写一点即可)

【答案】 锥形瓶 2KClO3![]() 2KCl + 3O2↑ AD BEG CaCO3 +2HCl==CaCl2 + CO2↑+H2O m 试纸a端变成红色 二氧化碳与水反应生成了碳酸 控制反应的停止和发生
2KCl + 3O2↑ AD BEG CaCO3 +2HCl==CaCl2 + CO2↑+H2O m 试纸a端变成红色 二氧化碳与水反应生成了碳酸 控制反应的停止和发生
【解析】本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的性质等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)据图可以看出,①是锥形瓶;
(2)实验室用氯酸钾和二氧化锰的固体混合物加热生成氯化钾和氧气,该反应的化学方程式为2KClO3![]() 2KCl + 3O2↑;要收集一瓶较纯净的氧气应选用排水法,所以收集一瓶较纯净的气体,选用的发生和收集装置是AD;
2KCl + 3O2↑;要收集一瓶较纯净的氧气应选用排水法,所以收集一瓶较纯净的气体,选用的发生和收集装置是AD;
(3)注射器可控制液体滴加速度,能控制反应的速度。要装配一套“控制反应速度”的气体发生装置,可用BEG;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式是:CaCO3 +2HCl==CaCl2 + CO2↑+H2O;二氧化碳的密度比空气大,可用排空气法收集,采用C装置是应从m端通入CO2;
(4)二氧化碳本身不呈酸性,二氧化碳与水反应生成了碳酸,碳酸呈酸性,所以试纸a端变成了红色;
(5)通过挤捏或放开塑料管,可以控制液体与固体的接触或分离,可以控制液体与固体的接触或分离的速度。该实验设计的优点有:能控制反应速率和控制反应的停止和发生。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究。
Ⅰ.固体的成分分析
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液的pH=7。
③碱石灰是CaO和NaOH的混合物
【提出猜想】猜想Ⅰ:固体未变质,只有NaOH
猜想Ⅱ:固体全部变质,只有Na2CO3
猜想Ⅲ:固体部分变质,是NaOH 和Na2CO3 的混合物
【原因分析】氢氧化钠在空气中变质的原因是_______________(用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是________________,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
同学 | 小钱 | 小徐 | 小陆 |
实验操作 | 加入适量氢氧化钙溶液 | 加入过量氯化钙溶液 | 逐滴加入稀盐酸至过量 |
【实验结论】小钱、小徐的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都得出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小钱的实验操作和现象无法确定猜想Ⅲ正确,理由是__________________。
(二)根据小徐的结论推测小陆实验现象是_________________________________。
Ⅱ 固体中各成分含量
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【进行实验】化学小组同学设计了如下实验装置。
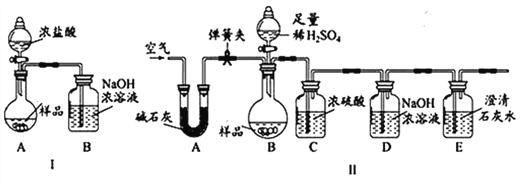
(一)小陆同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是 _______________________;
(二)小钱同学在大家讨论的基础上,设计了装置II。请分析:装置II中A的作用_____________;若无装置C,对测定结果造成的影响是_____________(填“偏大”、“偏小”或“无影响”);E装置的作用是_______________________________。
【实验结论】称取10g样品于圆底烧瓶中,实验结束后,测得装置D增重2.2g,请你计算出样品中Na2CO3质量分数为____________。(写出计算过程)
【反思评价】(一)实验室中的氢氧化钠应密封保存,除了因为空气中有二氧化碳,还因为___________。
(二)若将上述5g氢氧化钠固体全部溶解在45g水中,得到的溶液中氢氧化钠质量分数______10%(填“大于”、“小于”或“等于”)。