��Ŀ����
����Ŀ��ʵ����ij�����Һ�����������ͭ��Һ��ɡ�̽��С��ͬѧ����������ʵ�飺ȡ124.5g�û����Һ���ձ��У�Ȼ��120gNaOH��Һ�����μ������У�ÿ�γ�ַ�Ӧ�����������Һ�������������������������±���ʾ��
��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� | |
����NaOH��Һ������/g | 20 | 20 | 20 | 20 | 20 | 20 |
��Ӧ����Һ������/g | 144.5 | 164.5 | 179.6 | 189.8 | 200 | 220 |
ÿ�β�������������/g | 0 | 0 | m | n | 9.8 | 0 |
���㣺��1�����������в���������������m��_____��n��_____
��2������NaOH��Һ�����ʵ�����������_____
��3����5�μ���NaOH��Һ��ַ�Ӧ��������Һ�����ʵ�����������_____
���𰸡�4.9 9.8 40% 35.5%
��������
�⣺����������������
��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� | |
����NaOH��Һ������/g | 20 | 20 | 20 | 20 | 20 | 20 |
�����������ƺ�û��Ӧʱ�������� | 144.5 | 164.5 | 184.5 | 199.6 | 209.8 | 220 |
��Ӧ����Һ������/g | 144.5 | 164.5 | 179.6 | 189.8 | 200 | 220 |
�����仯 | 0 | 0 | 4.9 | 9.8 | 9.8 | 0 |
ÿ�β�������������/g | 0 | 0 | m | n | 9.8 | 0 |
��֪����ʼ���������ƺ����ᷴӦ���������������ƺ�����ͭ��Ӧ����������ͭ�������ҵ����ʵ����ǡ����ȫ��Ӧ���������������в���������������m��4.9��n��9.8��
���ݵ��Ĵ�ʵ��������������NaOH��Һ�����ʵ�����������
������NaOH��Һ�����ʵ���������Ϊx
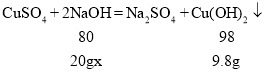
![]()
x��40%
�����μ���NaOH��Һ��ַ�Ӧ��������Һ�����ʵ���������Ϊy
��ʱ������Һ������Ϊ200g
������Ԫ���غ�ɵù�ϵΪ
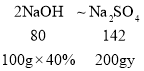
![]()
y��35.5%
�ʴ�Ϊ��
��1��4.9��9.8��2��40%����3��35.5%��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�