题目内容
【题目】小强买一包纯碱,包装如图,进行实验:准确称取5.5g样品放入烧杯中,向其中滴加盐酸至刚好完全反应(忽略CO2溶于水),共用去稀盐酸25g,得到溶液质量为28.3g(注:杂质溶于水,且与盐酸不反应。)求:

(1)生成CO2的质量为_________;
(2)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符。________(计算结果精确到0.1%)
【答案】 2.2g 经计算,碳酸钠的质量分数为96.4%,与包装说明不符
【解析】(1)生成二氧化碳的质量为:25g+5.5g28.3g=2.2g;(2)设碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
![]() ,解得:x=5.3g
,解得:x=5.3g
碳酸钠的质量分数为: ![]() =96.4%<98%,不符合说明。
=96.4%<98%,不符合说明。
答为:(1) 生成CO2的质量为2.2g;(2)纯碱样品中碳酸钠的质量分数与包装说明不相符。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学兴趣小组对“锌与稀硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】①可能与稀硫酸的溶质质量分数有关;②可能与锌的形状有关。
【设计并实验】兴趣小组用100mL不同质量分数的稀硫酸和5g不同形状的锌进行如下实验(时间为3分钟)。

(1)锌与硫酸反应的化学方程式为_______________________________。
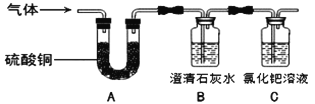
(2)如图所示装置收集并测量氢气的体积,则正确的链接顺序是:
氢气→______________________(填导管口序号)。
【收集证据】
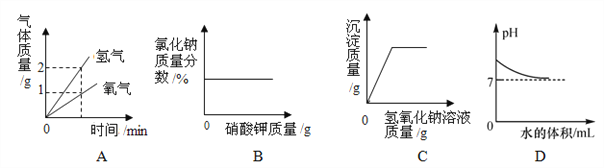
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是______。
【得出结论】依据上表得出的结论是____________________________________。
【反思评价】
(4)下表是兴趣小组第①组实验根据前6分钟记录详细数据(每分钟记录一次产生氢气的体积)。
时段 (均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积/mL | 3.1 | 16.7 | 11.9 | 9.6 | 7.6 | 6.0 |
请解释锌与稀硫酸反应由快变慢的原因____________________________________。
(5)锌与硫酸反应的快慢可能还会受_____________因素影响,如果用实验验证该因素对反应快慢的影响,应该控制________________因素不同,而其他因素则相同。
【题目】在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(设计实验)
(1)探究稀硫酸与氢氧化钠溶液的反应:
当滴入几滴酚酞试液后,溶液由无色变为________色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:_____________________.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是__________(填“方案一”或“方案二”)另外一个实验方案错误的原因是________________________;
(实验延伸)请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是____________,实验现象及结论是________________________.
(交流与反思)下图是小明和老师一起向氢氧化钠溶液中逐渐滴入稀硫酸时用数字化实验测定的反应溶液温度和pH的变化曲线。请你思考:
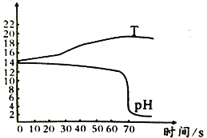
(1)为什么在0-60秒pH变化不大?_____________________;
(2)请仔细观察图2,从中获得的一条信息是_____________________。