题目内容
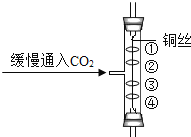
【题目】碳还原氧化铜的实验如图所示。写出该反应的化学方程式________________。
(提出问题)碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
(作出猜想)猜想①∶CO 猜想②∶CO2 猜想③∶________________。
(设计方案)实验装置如图(浓硫酸具有吸水作用)。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气∶
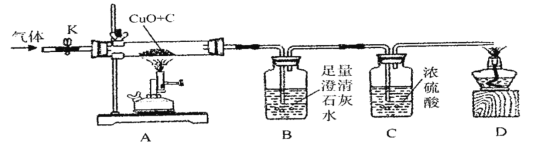
(1)实验时A处的现象是___________________。
(2)若猜想①成立,B、D处的现象是________________(填序号)。
aB中变浑浊,D处能点燃 bB中变浑浊,D处不能点燃
cB中无明显实验现象,D处能点燃 dB中无明显实验现象,D处不能点燃
方案二∶从定量计算角度判断
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据∶
反应前的质量 | 反应后的质量 | |
A(玻璃管+固体) | m1 | m2 |
B+C(广口瓶+混合液) | m3 | m4 |
(3)若猜想②成立,则理论上(m4一m3)__________(m1-m2)(选填“<”、“>”或“=”)。
(交流反思)实验开始前缓缓通入氮气的目的是_____________________。
【答案】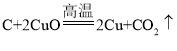 CO和CO2 黑色固体变红色 c = 排出装置内空气,防止加热时发生危险,防止空气中成分干扰
CO和CO2 黑色固体变红色 c = 排出装置内空气,防止加热时发生危险,防止空气中成分干扰
【解析】
高温条件下,氧化铜和碳反应生成铜和二氧化碳,该反应的化学方程式为: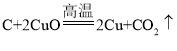
作出猜想:猜想①:CO 猜想②:CO2猜想③:CO和CO2
设计方案(1)实验时A处的氧化铜和碳反应生成铜和碳的氧化物,黑色固体变红色。
(2)若猜想①成立,一氧化碳不能和氢氧化钙反应,B中无明显实验现象,一氧化碳燃烧生成二氧化碳,D处能点燃。故选c。
方案二:
(3)若猜想②成立,氧化铜中的氧元素和碳中的碳元素转化成二氧化碳,被澄清石灰水吸收,(m4-m3)是吸收的二氧化碳质量,(m1-m2)是氧化铜中氧元素和碳中碳元素的质量和,则理论上(m4-m3)=(m1-m2)。
交流反思:实验开始前缓缓通入氮气的目的是排出装置内空气,防止加热时发生危险,防止空气中成分干扰。

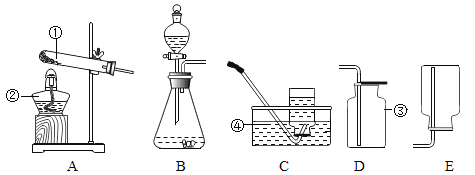
【题目】(一) 下图所示为实验室中常见的气体制备和收集装置.
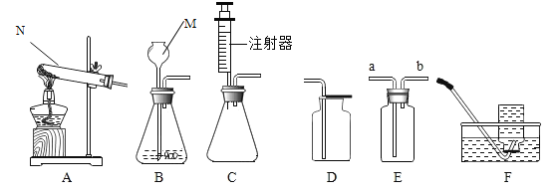
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用的发生装置是_____ (填字 母序号)。若用装置B制取二氧化碳,反应的原理是(用化学方程式表示)_____。
(2)实验室用H2O2溶液和MnO2制取氧气, 若选用C做发生装置,你认为选用C的优点是_____。
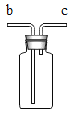
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从_____ (填“a”或“b”) 端通入:欲使用装置E.用排水法收集氧气,先将瓶中装满水,再将气体从_____ (填“a”或“b”) 端通入。
(4)已知一氧化氮气体难落于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置_____(填字母序号)。
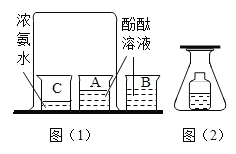
(二)小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,井向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应:②氢氧化钠有剩余:③盐酸过量。
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是:_____。
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
实验方法 | 可能观察到的现象 | 结论 |
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。 | 如果_____。 | 则盐酸过量 |
如果_____。 | 则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是_____。(填序号).
A 生锈的铁钉
B 碳酸钠粉末
C 硫酸钠粉末
D 氢氧化铜
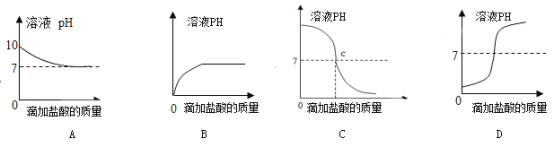
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是_____(填序号)。
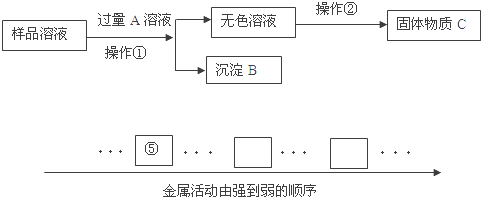
【题目】兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
(1)将金属R投入稀盐酸中,金属表面有气泡冒出.则该金属R在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
(2)为了比较金属R与铁的活动性强弱,兴趣小组设计下列方案进行实验,请完成下表:
你的一种猜想 | 验证方法 | 现象 | 结论 |
金属R的活动性比铁 | 将金属R投入 溶液中 | 金属R表面有黑色的物质析出 | 猜想 (选填“正确”或“错误”) |
(3)请根据上述的信息,标出金属Fe、R、Cu在下列金属活动性顺序表中的相应位置。
【题目】为测定石灰石样品的纯度,取4g该样品,将40g稀盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表。
次数 | 1 | 2 | 3 | 4 |
加入盐酸质量/g | 10 | 10 | 10 | 10 |
剩余固体质量/g | 2.5 | 1.0 | 0.4 | 0.4 |
(1)该石灰石样品中碳酸钙的质量分数是_____;
(2)求100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量_____。