��Ŀ����
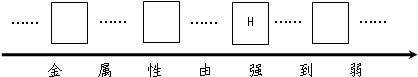
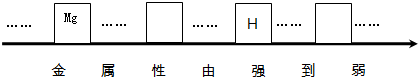
����ͭ����һ�ֽ���R������������þ�����е�һ�֣��Ļ�Ϸ�ĩ����ȷ��R�ijɷ֣�����һ����ɣ���1���뽫����þ�������ֽ�����Ԫ�ط�����д�����н������˳����е���Ӧλ�ã�
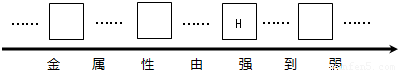
��2��ȡ�����Ľ�����ĩ���Թ��У���μ���ϡ���ᣬ�����ݲ�������R��������______��
��3�������ٲ�������ʱ���ٽ���______����дһ��ʵ��������������õ���Һ��ͭ��Ȼ������Һ�м���ྻ��пƬ��пƬ�����н�����������R��______��
��4��д������R��ϡ���ᷴӦ�Ļ�ѧ����ʽ______���÷�Ӧ�Ļ�����������______��ѡ����ϡ������ֽ⡱�����û������ֽ⡱����Ӧ��
���𰸡���������1�����ݽ������˳������þ�������ֽ�����Ԫ�ط�����������˳����е���Ӧλ�ã�
��2�����ݽ������ᷴӦ�Ĺ��ɣ��ɽ�����ĩ��ϡ���ᷴӦ�������ݲ������ƶϽ���R��
��3�����ݲ�����õ���Һ��ͭ�Ľ�����ж������е�ʵ����������ݽ������η�Ӧ���ɣ���пƬ�����н����������ƶϽ���R��
��4�����ݶԽ���R���ƶϣ�д�������ᷴӦ�Ļ�ѧ����ʽ�����Ը÷�Ӧ���з��࣮
����⣺��1����������þ�������ֽ����Ļ��ǿ����ϵþ�������⣾�������ж�˳�������˿ո���Ϊþ���������Ŀո���Ϊ�������Ҷ�Ϊ����
��2��ͭ����һ�ֽ���R�Ļ�Ϸ�ĩ����ϡ���ᷴӦ�ų����������жϽ���R�����ᷴӦ�����������ɽ���R�������ǽ�������
��3�����ݲ��������Һ��ͭ���뿪�������жϸò���Ϊ���ˣ�������Һ��������п��Ӧ�����ж����н�����Ա�п����������þ�Ļ�Ա�пǿ����˽���RӦΪ����
��4���������ᷴӦ����������������������ѧ����ʽΪFe+H2SO4=FeSO4+H2�����÷�ӦΪ�����뻯�������ɵ����뻯������û���Ӧ��
�ʴ�Ϊ��
��1��Mg��Fe��Ag��
��2��������Ag����
��3�����ˣ�������Fe����
��4��Fe+H2SO4=FeSO4+H2�����û���
�������������˳����λ����֮ǰ�Ľ����ܴ������û����⣬���ǿ�Ľ����ܽ�������Ľ�����������Һ���û�������
��2�����ݽ������ᷴӦ�Ĺ��ɣ��ɽ�����ĩ��ϡ���ᷴӦ�������ݲ������ƶϽ���R��
��3�����ݲ�����õ���Һ��ͭ�Ľ�����ж������е�ʵ����������ݽ������η�Ӧ���ɣ���пƬ�����н����������ƶϽ���R��
��4�����ݶԽ���R���ƶϣ�д�������ᷴӦ�Ļ�ѧ����ʽ�����Ը÷�Ӧ���з��࣮
����⣺��1����������þ�������ֽ����Ļ��ǿ����ϵþ�������⣾�������ж�˳�������˿ո���Ϊþ���������Ŀո���Ϊ�������Ҷ�Ϊ����
��2��ͭ����һ�ֽ���R�Ļ�Ϸ�ĩ����ϡ���ᷴӦ�ų����������жϽ���R�����ᷴӦ�����������ɽ���R�������ǽ�������
��3�����ݲ��������Һ��ͭ���뿪�������жϸò���Ϊ���ˣ�������Һ��������п��Ӧ�����ж����н�����Ա�п����������þ�Ļ�Ա�пǿ����˽���RӦΪ����
��4���������ᷴӦ����������������������ѧ����ʽΪFe+H2SO4=FeSO4+H2�����÷�ӦΪ�����뻯�������ɵ����뻯������û���Ӧ��
�ʴ�Ϊ��
��1��Mg��Fe��Ag��
��2��������Ag����
��3�����ˣ�������Fe����
��4��Fe+H2SO4=FeSO4+H2�����û���
�������������˳����λ����֮ǰ�Ľ����ܴ������û����⣬���ǿ�Ľ����ܽ�������Ľ�����������Һ���û�������

��ϰ��ϵ�д�
�����Ŀ
����ͭ����һ�ֽ���R�Ļ�����ĩ����һ�ֽ���R������þ������п�е�һ�֣��ֲⶨ����ɣ�ȡ�û�����ĩ16.0g�����ձ��У���140.0g 14.0%��ϡ������Ĵμ�����ձ��У���ַ�Ӧ���ʣ��������ݼ�¼��
ͨ�����㣨д��������̣�����������1λС��������
��1���û�����ĩ����һ����RΪ���ֽ�����
��2�������μ���ϡ�����ַ�Ӧ��������Һ�����ʵ����������Ƕ��٣�
| ���� | 1 | 2 | 3 | 4 |
| ����ϡ���������/g | 35.0 | 35.0 | 35.0 | 35.0 |
| ʣ����������/g | 12.75 | 9.5 | 6.25 | 5.6 |
��1���û�����ĩ����һ����RΪ���ֽ�����
��2�������μ���ϡ�����ַ�Ӧ��������Һ�����ʵ����������Ƕ��٣�