题目内容
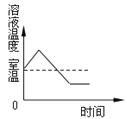
【题目】如图是甲、乙、丙三种物质的溶解度曲线。下列判断不正确的是
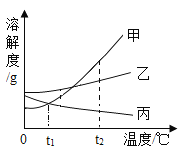
A.t2℃丙的饱和溶液温度降低变为不饱和溶液
B.三种物质中,溶解度随温度变化最明显的是甲
C.t2℃甲的饱和溶液温度降低,溶质的质量分数减小
D.甲和乙的饱和溶液分别由t2℃降到t1℃,乙析出晶体的质量比甲的多
【答案】D
【解析】
A、根据题目信息可以看出,丙的溶解度随温度的降低而增大,随温度升高而降低,所以在t2℃时丙为饱和溶液,降低温度后丙的溶解度增大,所以降低温度后变为不饱和溶液,选项A正确;
B、甲的溶解度曲线随温度变化较大,所以甲的溶解度受温度影响较大,选项B正确;
C、甲的溶解度随温度降低而降低,所以在t2℃时甲的饱和溶液温度降低后,溶质析出,溶质减小,所以溶质质量分数变小,选项C正确;
D、甲的溶解度变化大于乙的,在等质量饱和溶液状态下,降低温度后甲析出的晶体较多,甲析出晶体质量大于乙的,但是此处未提及饱和溶液质量,所以无法比较析出固体质量,选项D不正确。故选D。

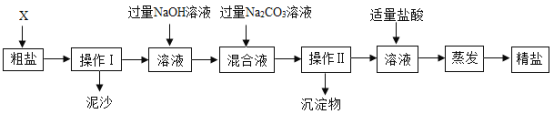
【题目】某同学用Ca(OH)2和Na2CO3溶液来制取NaOH,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
[提出问题]:滤液中溶质的成分是什么?
[猜想与假设]:猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:______(将猜想三补充完整)
[设计并实验]:对可能存在的溶质,需进一步实验验证。
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想_____不成立 |
实验二 | 另取少量滤液于试管中,向其中滴入适量碳酸钠溶液 | _____ | 猜想三成立,发生反应的化学方程式为______ |
【题目】请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
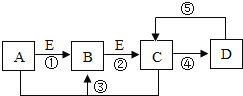
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
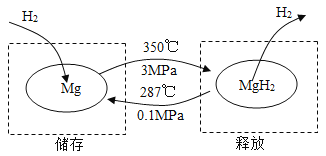
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |