题目内容
【题目】图1是甲、乙两种物质的溶解度曲线,请回答问题:

(1) ℃时,甲、乙两种物质的溶解度相等.
(2)溶解度随温度升高而降低的物质是 (填“甲”或“乙”).
(3)可使甲物质从其饱和溶液中结晶析出的方法是 .
(4)t1℃时,分别将甲、乙两种物质的饱和溶液升温到t2℃,甲溶液的溶质质量分数 (填“大于”、“等于”或“小于”)乙溶液的溶质质量分数.
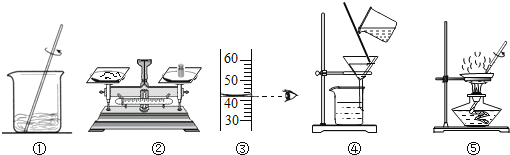
(5)小明同学用甲物质进行以下实验如图2:
①实验过程中,B、C、D对应的溶液为不饱和溶液的是如图2 .
②向B对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出.你认为“全部溶解”的原因是 .
【答案】(1)t1;(2)乙;(3)降低温度;(4)大于;(5)①B;②甲溶于水时放出热量.
【解析】
试题分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)根据物质的溶解度曲线可以判断物质的溶解度随温度变化情况;
(3)根据物质的溶解度随温度变化情况可分析提纯物质的方法;
(4)据饱和溶液中溶质的质量分数计算方法及甲乙溶解度随温度变化情况分析解答;
(5)根据加入物质的质量和不同温度下甲的溶解度分析判断;
向B对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出,可能是甲溶于水时放热.
解:(1)t1℃时,甲、乙两种物质的溶解度相等;
(2)由图可知:乙的溶解度随温度升高而减小;
(3)降低温度适合溶解度随温度升高而增大且受温度影响大的固体,t1℃时甲的溶解度是65g,t2℃时甲的溶解度是90g;说明甲的溶解度随温度的升高而增大,所以可使甲物质从其饱和溶液中结晶析出的方法是降低温度;
(4)从题中信息可知:t1℃时二者的溶解度相等,据饱和溶液中溶质的质量分数=![]() ×100%,可知溶解度相等则溶质的质量分数相等,升温后甲的溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数不变,乙的溶解度减小,析出晶体,溶质的质量分数减小,所以升温后甲的质量分数大于乙;
×100%,可知溶解度相等则溶质的质量分数相等,升温后甲的溶解度增大,溶液中溶质、溶剂的质量不变,溶质的质量分数不变,乙的溶解度减小,析出晶体,溶质的质量分数减小,所以升温后甲的质量分数大于乙;
(5)①在t1℃时二者的溶解度是65g,即100g水最多溶解甲、乙都是65g,该温度下50g水中溶解32.5g甲才饱和,所以图中B溶解20g甲得到的是甲的不饱和溶液;C中一共加入50g甲只能溶解32.5g,所以得到的C是饱和溶液;t2℃时100g水最多溶解甲是90g所以该温度下50g水中最多溶解45g,一共加入50g甲不能全部溶解得到的是饱和溶液;
②在t1℃时100g水最多溶解甲、乙都是65g,该温度下50g水中溶解32.5g甲就饱和,温度不变的话50g甲不能全溶,却发现固体全部溶解,一段时间后又有部分固体析出,而甲的溶解度随温度的升高而增大,所以开始能全溶说明温度升高,说明甲溶于水放热使温度升高固体溶解,温度冷却后溶解度减小又析出固体;
故答案:(1)t1;(2)乙;(3)降低温度;(4)大于;(5)①B;②甲溶于水时放出热量.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案