题目内容
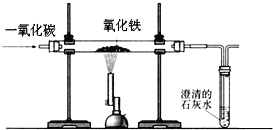
【题目】通过一年的化学学习,相信你已经初步掌握了实验室制取气体相关实验操作的有关知识,请结合图示回答问题:

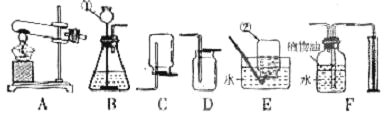
(1)写出图中仪器a、b的名称:a ,b .
(2)实验室用装置B制取CO2时,如用注射器替换长颈漏斗,优点是 .
(3)实验室加热氯酸钾制取氧气的化学方程式是 ,应选择的发生装置是 ,若用盛满水的F装置收集氧气,应从导管 (填①或②)通入.
(4)氨气是一种有刺激性气味、易溶于水、密度比水小的气体,实验室用加热氯化钠和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是 .
(5)小明在实验室里加热31.6g高锰酸钾制取氧气,完全反应后剩余固体质量为28.4g,将剩余固体溶解、过滤、烘干、回收二氧化锰.
请计算:①生成氧气的质量.②回收二氧化锰的质量.
【答案】(1)试管;集气瓶;
(2)可控制反应速率,又可节约药品;
(3)2KClO3![]() 2KCl+3O2↑;A;②;
2KCl+3O2↑;A;②;
(4)AE;
(5)答:①生成氧气的质量是3.2g.②回收二氧化锰的质量是8.7g.
【解析】
试题分析:(1)根据常用仪器回答;
(2)注射器可控制液体的滴加速率,进而可控制反应速率,节约药品;
(3)据反应原理书写方程式,该反应属于固体型,故选发生装置A,氧气密度比水小,所以应从短管进气,长管便于排水;
(4)据反应物状态和反应条件选择发生装置,据气体密度和溶解性选择收集装置;
(5)据高锰酸钾分解的反应原理可知:反应中减少的固体的质量即是生成的氧气的质量,并据氧气的质量计算出二氧化锰的质量.
解:(1)标号仪器分别是试管和集气瓶;
(2)注射器可控制液体的滴加速率,进而可控制反应速率,需要氧气时滴加液体,不需要时,不再滴加,故还能节约药品;
(3)加热氯酸钾和二氧化锰的混合物生成氯化钾和氧气,二氧化锰是反应的催化剂,反应方程式是:2KClO3![]() 2KCl+3O2↑,该反应属于固体型,故选发生装置A,氧气密度比水小,所以应从短管进气,长管便于排水;
2KCl+3O2↑,该反应属于固体型,故选发生装置A,氧气密度比水小,所以应从短管进气,长管便于排水;
(4)用加热氯化钠和熟石灰的固体混合物的方法制取氨气,该反应属于固体加热型,故选发生装置A,氨气密度比空气小且极易溶于水,所以只能用向下排空气法收集;
(5)依据质量守恒定律,生成氧气的质量是:31.6g﹣28.4g=3.2g;
设生成二氧化锰的质量是x
2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
87 32
x 3.2g
![]() =
=![]()
x=8.7g
故答案为:(1)试管;集气瓶;
(2)可控制反应速率,又可节约药品;
(3)2KClO3![]() 2KCl+3O2↑;A;②;
2KCl+3O2↑;A;②;
(4)AE;
(5)答:①生成氧气的质量是3.2g.②回收二氧化锰的质量是8.7g.

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案