题目内容
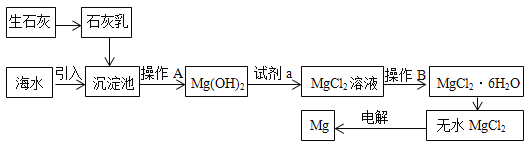
【题目】(I)金属镁广泛应用于生活、生产和国防工业。从海水或卤水中提取镁的流程如下:
①操作A的名称是_______,操作B的名称是__________。
②试剂a的化学式为__________;无水MgCl2电解反应后的另一产物是________。
(II)A~H都是初中化学常见物质。其中A、B的组成元素相同,且常温下都是无色液体;H是蓝色沉淀。X、Y都是氧化物,其中X是黑色粉末状固体,Y常用作食品干燥剂,Z是红色固体。它们之间有如图转化关系。
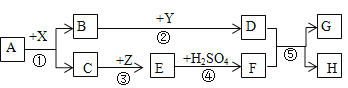
根据上述信息,回答下列问题:
(1)A的化学式为 ______ ;A在医疗上常用作_________ 。
(2) 反应②中伴随着______(填“放热”或“吸热”)现象;Z的一种用途是_____。
(3)反应⑤的化学方程式为 _____ ;在反应①②③④⑤中属于化合反应的有_______。
【答案】过滤 加热浓缩(蒸发或蒸发结晶) HCl Cl2(或氯气) H2O2 消毒剂(或消毒) 放热 作导线 CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4 ②③
【解析】
A、B的组成元素相同,且常温下都是无色液体,A可以生成B,故A为过氧化氢,B为水,C为氧气;其中X是黑色粉末状固体为二氧化锰,Y常用作食品干燥剂,还是氧化物,故Y为氧化钙,氧化钙和水生成氢氧化钙,故D为氢氧化钙,Z是红色固体故为铜和氧气反应生成氧化铜,故E为氧化铜,氧化铜和硫酸反应生成硫酸铜,故F为硫酸铜,硫酸铜和氢氧化钙生成氢氧化铜沉淀和硫酸钙,H是蓝色沉淀为氢氧化铜,G为硫酸钙。代入转化关系,符合题意。
(I)(1)固液分离操作是过滤,通过蒸发氯化镁得到氯化镁结晶水合物,故填:过滤;加热浓缩(蒸发或蒸发结晶)。
(2)氢氧化镁和稀盐酸反应生成氯化镁和水,氯化镁电解生成镁和氯气,故填:HCl;Cl2。
(II)(1)有分析可知A为过氧化氢,医疗上常用作消毒剂,化学式为H2O2,故填:H2O2;消毒剂。
(2)反应②为氧化钙和水生成氢氧化钙,该反应放热,由分析由分析可知Z为铜,可用作导线,故填:放热;作导线。
(3)由分析可知反应在反应①②③④⑤分别是过氧化氢分解生成氧气和水,氧化钙和水生成氢氧化钙,铜和氧气生成氧化铜,氧化铜和硫酸生成硫酸铜和水,⑤硫酸铜和氢氧化钙反应生成硫酸钙和氢氧化铜沉淀化学方程式为CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4,其中②③符合“多变一”特点属于化合反应,故填:CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4 ; ②③。

【题目】甲同学对有关盐的知识进行了以下的整理.
(1)填写下表空格中的化学式:
氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
______ | CaCl2 | NaCl | MgCl2 | AlCl3 | ______ | ______ | ______ |
反思:①以上盐中的金属元素的排列,可以得出是依据____顺序归纳整理的.
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液是否会具有相似的化学性质?____为什么?_____
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成图.验证:请写出下列有盐生成的部分化学方程式:
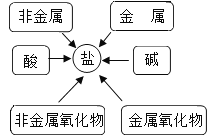
①用稀硫酸除铁锈_____;
②盐酸和氢氧化钠反应_____;属于____反应
③古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液,化学方程式为_____;属于_____反应.
(3)甲同学在整理碳酸盐知识时,探究实验室用碳酸钙粉末、碳酸钠或碳酸氢钠,制取CO2的方法.
提出问题:实验室通常使用下列装置![]() 制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是_____.
制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是_____.
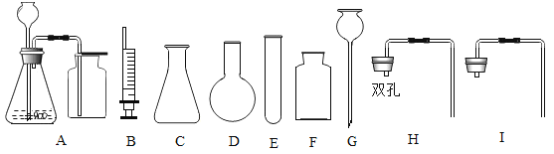
实验设计:通过控制反应物的用量来得到平稳的CO2气流的目的.因此,用碳酸盐粉末制取CO2的发生装置,可以选择_____(填仪器编号)组装.
(4)向16.8g碳酸氢钠粉末中,缓缓加入100g稀盐酸,如恰好完全反应,计算生成CO2的质量和反应前稀盐酸中溶质的质量分数_____.(请在答卷纸上写出计算过程)
【题目】学习盐的化学性质时,进行了如图所示的实验(提示:氯化钙、氯化钡的溶液都呈中性):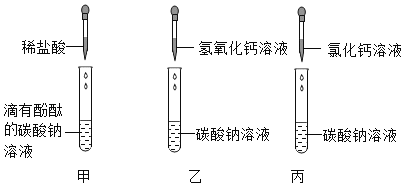
(1)碳酸钠是一种重要的盐,甲中碳酸钠溶液中加入酚酞,溶液显_____色;乙中发生反应的化学方程式是______________________。
(2)实验结束后,将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,过滤,得到滤液,滤液中一定不含有_______。
(3)对滤液中溶质进行探究。
(实验猜想)所得滤液中溶质可能为:
猜想一:NaCl、Na2CO3; 猜想二:NaCl、CaCl2
猜想三:NaCl、Na2CO3和NaOH; 猜想……
小明提出猜想二一定不成立,原因是_____________________________。
(实验设计)
实验操作 | 实验现象 | 实验结论 |
取少量滤液于试管中,加入过量BaCl2溶液 | ____________ | 猜想三成立 |
(实验分析)在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑_______。
【题目】某地曾发生了一起亚硝酸钠中毒事件。亚硝酸钠外观酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如下:
项 目 | 亚硝酸钠 | 氯化钠 |
水溶性 | 易溶,在15℃时溶解度为81.5g | 易溶,在15℃时溶解度为35.8g |
熔 点 | 271℃ | 801℃ |
沸 点 | 320℃会分解,放出有臭味的气体 | 1413℃ |
跟稀盐酸作用 | 放出红棕色的气体 | 无反应 |
(1)根据上表,请你写出亚硝酸钠的两个物理性质:①_____,②________;
(2)检验亚硝酸钠的方法可以是:_____。