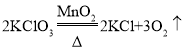题目内容
【题目】工业上以白云石(主要成分为CaCO3和MgCO3)为原料制备氢氧化镁的流程如图所示,请回答以下问题:

资料卡片:
①轻烧时温度低于700 °C;
②![]() ;
;
③![]() ;
;
④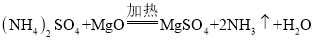
(1)白云石轻烧后所得固体的主要成分是__________。
(2)流程中研磨的目的是____________。
(3)流程中除水以外可以循环利用的物质是________。
(4)流程中最后一个步骤是向硫酸镁溶液中通入氨气,反应生成氢氧化镁沉淀和硫酸铵,该反应的化学方程式是_________。
(5)如果轻烧时温度超过700 °C ,对流程产生的影响是____________。
【答案】CaCO3和MgO 增大反应物之间的接触面积,加快反应 (NH4)2SO4和NH3 ![]() 温度超过700 °C .碳酸钙发生分解反应生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,影响生成物的纯度
温度超过700 °C .碳酸钙发生分解反应生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,影响生成物的纯度
【解析】
(1)由题意可知,轻烧时的温度低于700 °C,此时白云石中的碳酸镁分解生成氧化镁和二氧化碳,而碳酸钙不发生反应,所以白云石轻烧后所得固体的主要成分是CaCO3和MgO,故填CaCO3和MgO。
(2)研磨可将块状固体研成粉末,增大了固体的表面积,进而增大了反应物之间的接触面积,能够加快反应,故填增大反应物之间的接触面积,加快反应。
(3)由流程图可知,生产过程中,既有硫酸铵和氨气参加的反应,也有生成硫酸铵和氨气的反应,所以流程中除水以外可以循环利用的物质还有(NH4)2SO4和NH3,故填(NH4)2SO4和NH3。
(4)该反应是硫酸镁、水和氨气反应生成氢氧化镁沉淀和硫酸铵,故反应的化学方程式写为MgSO4+2NH3+2H2O=Mg(OH)2↓+(NH4)2SO4。
(5)如果温度超过700 °C ,碳酸钙就会发生分解反应生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,从而影响生成物的纯度,故填温度超过700 °C,碳酸钙发生分解反应生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,影响生成物的纯度。

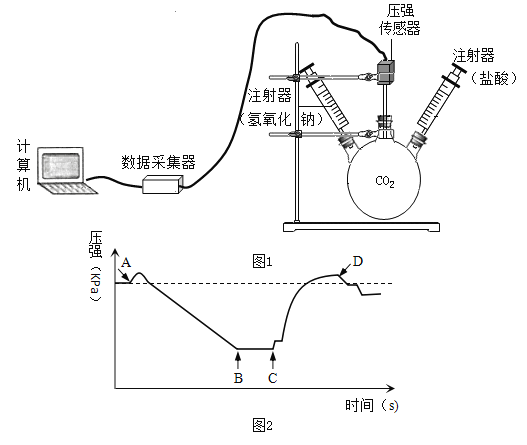
【题目】二氧化碳与氢氧化钠溶液反应没有明显现象,某兴趣小组设计如下图所示的实验装置,欲证明二氧化碳与氢氧化钠发生反应。
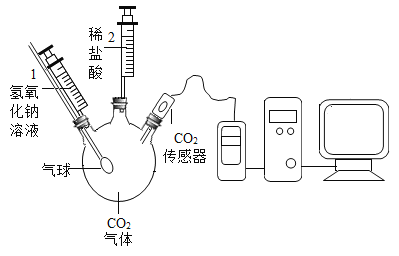
实验序号 | 实验操作 | 实验现象 |
① | 启动CO2传感器 | |
② | 将注射器1中的溶液推入充有CO2的瓶中 | 气球胀大 |
③ | 将注射器2中的溶液推入瓶中 | ________ |
(1)实验是从定量的角度验证二氧化碳与氢氧化钠的反应,绘制曲线图象如图所示:
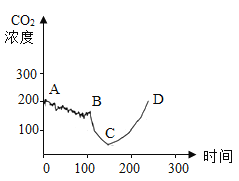
BC段发生反应的化学方程式为_________(假设氢氧化钠过量) ,CD段CO2浓度增大的原因是___________。
(2)实验结束后,向剩余的溶液中滴加酚酞溶液,发现溶液变成红色。同学们对这一现象产生了兴趣。
[提出问题]剩余溶液中,能使溶液呈碱性的物质是什么?
[猜想假设]小亮认为:只有碳酸钠
小红认为:只有氢氧化钠
小华认为:二者可能都有
[查阅资料]①同等条件下,中和反应优于酸和碳酸盐的反应
②氯化钙(或氯化钡)溶液呈中性
[交流讨论]同学们讨论后认为小红和小华的猜想均不成立。理由是__________。
[实验设计]小亮设计了如下实验,通过实验证明自己的猜想是正确的。
实验操作 | 实验现象 | 实验结论 |
①__________ | ________ | 小亮的猜想正确 |
②充分反应后,滴加几滴无色酚酞试液 | 溶液不变色 |
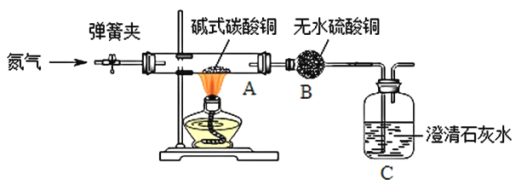
【题目】工业上用电解饱和食盐水的方法制备烧碱(NaOH)、氯气(Cl2)和氢气,并以它们为原料生产一系列化工产品,称为氯碱工业,某化学兴趣小组同学在实验室进行如下探究:
探究一:验证电解饱和食盐水的产物
(查阅资料)(1)氯气在通常情况下呈黄绿色、是一种有强烈刺激性气味的有毒气体;(2)氯气能与碱溶液发生反应,能使湿润的淀粉碘化钾试纸变蓝。
(实验验证)按图甲所示装置进行实验探究
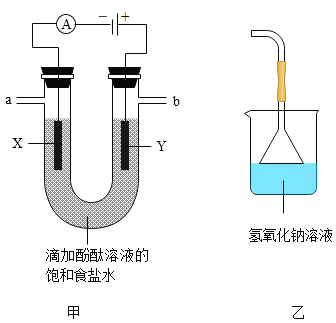
接通电源一段时间后,观察到X、Y电极周围均有气泡产生,溶液由无色变为红色。用小试管在a端收集气体,移近酒精灯火焰,松开拇指,发出轻微的爆鸣声。将湿润的淀粉碘化钾试纸放在b端,试纸变蓝。
(实验分析)
(1)a端收集到的气体是_____。
(2)电解饱和食盐水的化学方程式为_____。
(3)b端后连接乙装置,乙装置中氢氧化钠溶液的作用是_____。
(拓展延伸)上述电解饱和食盐水实验中,电解产物之间能发生化学反应。为避免产物混合发生反应,工业上常用离子交换膜法进行生产制备,将得到的溶液蒸发结晶获得烧碱。
探究二:工业上生产的烧碱中含有哪些杂质?
(猜想假设)
猜想一:NaCl
猜想二:Na2CO3
猜想三:NaCl和Na2CO3
工业上生产的烧碱中可能含有Na2CO3,作出此猜想的依据是_____。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液 | _____ | 猜想三正确 |
(反思评价)
(1)小乐同学认为上述实验中可用稀盐酸代替稀硝酸,小娟不同意,小娟的理由是_____,
(2)除去烧碱溶液中少量的碳酸钠,可选用的药品是_____ (填标号)。
A CuCl2溶液
B Ba(NO3)2溶液
C Ba(OH)2溶液
D KOH溶液