题目内容
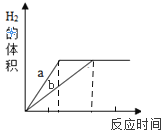
【题目】烧杯中盛有FeCl2和CuCl2的混合溶液,逐渐加入足量的锌粒,溶液的质量和加入锌粒的质量关系如图所示,回答下列问题:
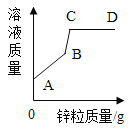
(1)写出AB段发生反应的化学方程式_________
(2)B点溶液中含有的溶质是什么_________?
(3)D点对烧杯中的物质进行过滤,向得到的滤渣中加盐酸现象是什么_________?
【答案】![]() ZnCl2 、 FeCl2 滤渣部分溶解并有气泡产生
ZnCl2 、 FeCl2 滤渣部分溶解并有气泡产生
【解析】
根据金属活动性顺序表可知,金属活动性Zn>Fe>H>Cu。所以锌先和氯化铜反应生成氯化锌和铜。完全反应后,锌再和氯化亚铁反应生成氯化铁和锌。
(1)根据上述分析可知,AB段是锌和氯化铜反应生成氯化锌和铜。故答案为:![]() ;
;
(2)B点表示氯化铜刚好完全反应,所以此时溶液中含有的溶质是氯化锌、氯化亚铁。故答案为:ZnCl2、FeCl2;
(3)根据上述分析可知,D点时锌过量,所以此时滤渣中含有锌、铁、铜。而锌和铁能与稀盐酸反应生成气体,铜不反应,所以能观察到滤渣部分熔接,有气泡产生。故答案为:滤渣部分溶解并有气泡产生。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】某化学兴趣小组的同学,为了判断某铁合金是生铁还是钢。取该铁合金8.6克(已知合金中只含铁、碳元素)于烧杯中,将80克稀酸分四次加入,充分反应,测得实验数据如下表所示。
一 | 二 | 三 | 四 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 28.5 | 48.4 | 68.3 | 88.3 |
(1)铁合金完全反应生成氢气的总质量为_____克;
(2)请通过计算判断。该铁合金属于生铁还是钢?_____