题目内容
【题目】(1)某化学兴趣小组的同学向无水乙醇中放入一小块金属钠,观察到有气泡产生。小组同学对这一现象产生了兴趣,进行了如下探究
(提出问题)无水乙醇和金属钠反应产生的气体是什么?
(查阅资料)I无水乙醇(CH3CH2OH)和金属钠反应生成乙醇钠CH3CH2ONa)和一种常见的可燃性气体;
Ⅱ浓硫酸具有较强的吸水性,可用作某些气体的干燥剂,比
Ⅲ白色的无水硫酸铜粉末遇水后会变成蓝色。
(猜想与假设)猜想一:CO;猜想二:CH4;猜想三:H2。兴趣小组的同学提出上述猜想的理论依据是_______________
(设计并实验)兴趣小组的同学分成甲、乙两组设计实验方案进行探究。
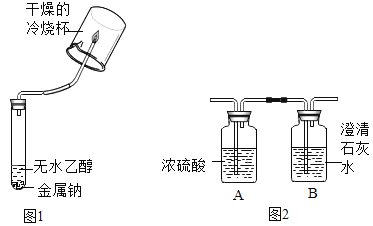
①甲组同学设计的实验方案如下:
实验操作 | 实验现象 | 实验结论 |
将反应产生的气体点燃在火焰上方罩一个干燥的冷烧杯 | 烧杯内壁有小液滴生成 | 猜想三成立 |
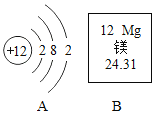
②乙组同学认为只完成上述实验猜想二也可能成立理由是 _________,并设计了如下实验进一步验证:将反应产生的气体点燃,燃烧产物依次通人A、B装置(如图2),测得A装置中质量增大,B装置中质量不变乙组的同学根据实验数据分析,证明猜想_________成立
(得出结论)无水乙醇与金属钠反应的化学方程式为_____________;该反应的基本反应类型是____________。
(实验反思)甲组同学受到乙组同学的启发认为只需要增加一个实验:再在火焰上方罩一个内壁蘸有澄清石灰水的烧杯,观察现象,就能使本组的实验方案更加完善。你认为此方案________ (选填“合理”或“不合理”)。
(拓展延伸)要确认该实验过程中所用的乙醇是无水乙醇的实验方法是____________。
(2)小明同学为了测定实验室中一瓶标签破损的硫酸的溶质质量分数,他取20g该硫酸于烧杯中,向其中加入10g锌粉(锌粉过量),完全反应后测得烧杯内物质的总质量为29.9g。该瓶硫酸的溶质质量分数是___________?
【答案】质量守恒定律 甲烷燃烧也能生成水 三 2CH3CH2OH+2Na=2CH3CH2ONa+H2↑ 置换反应 合理 取样,加入无水硫酸铜固体,颜色无变化,证明是无水乙醇 24.5%
【解析】
(1)[猜想与假设]兴趣小组的同学提出上述猜想的理论依据是质量守恒定律,即反应前后元素种类不变;
[设计并实验]②甲烷燃烧生成二氧化碳和水,所以将反应产生的气体点燃在火焰上方罩一个干燥的冷烧杯,烧杯内壁有小液滴生成;乙组同学认为只完成上述实验,猜想二也可能成立。
B装置中质量不变,说明反应没有生成二氧化碳,A装置质量增大,说明反应生成了水,即气体是氢气,证明猜想三成立;
[得出结论]无水乙醇与金属钠反应生成乙醇钠和氢气,反应的化学方程式为:2CH3CH2OH+2Na=2CH3CH2ONa+H2↑.反应是一种化合物和一种单质反应生成另外一种化合物和另外一种单质,属于置换反应;
[实验反思]在火焰上方罩个内壁蘸有澄清石灰水的烧杯,如果澄清石灰水变浑浊,说明生成了二氧化碳,反之则没有生成二氧化碳,所以可以分别验证是否有水和二氧化碳生成,因此此方案合理合理;
[拓展延伸]白色固体无水硫酸铜能和水反应生成蓝色固体五水硫酸铜,利用这一特点可以:取样,加入无水硫酸铜固体,颜色无变化,证明是无水乙醇;
(2)氢气的质量为20g+10g-29.9g=0.1g,设硫酸的质量是x,
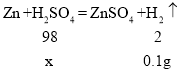
![]()
x=4.9g,
该瓶硫酸的溶质质量分数是![]() ×100%=24.5%,
×100%=24.5%,
答:该瓶硫酸的溶质质量分数是24.5%。

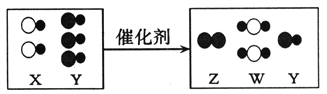
【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 2.2 | 6.4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 3.6 | 2.2 | a |
下列判断正确的是( )
A. 表中a的值为2.8 B. X可能是该反应的催化剂
C. X不可能含有氢元素 D. X只含碳元素
【题目】小樱同学用如图所示装置,分别进行“燃烧条件”和“氧气性质”的探究实验(已如:白磷的着火点为40℃),请回答下列问题。
内容步骤 | (实验1)燃烧条件 | (实验2)氧气性质 |
步骤1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞; | 烧杯中盛有Ca(OH)2溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞; |
步骤2 | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
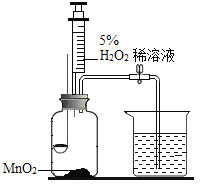
(1)H2O2与MnO2接触时,发生反应的化学方程式为________,MnO2的作用是______。
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,燃烧匙中的白磷不燃烧的原因是______;水中的白磷不燃烧的原因是_______。打开止水夹,烧杯中观察到的现象是______。
(3)实验2中,打开止水夹,推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是______,木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶中,集气瓶中观察到的现象是______。