题目内容
【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 2.2 | 6.4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 3.6 | 2.2 | a |
下列判断正确的是( )
A. 表中a的值为2.8 B. X可能是该反应的催化剂
C. X不可能含有氢元素 D. X只含碳元素
【答案】AC
【解析】A、根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则可求出a的质量=2.2+6.4-2.2-3.6=2.8,正确;B、X在反应前质量为0,而反应后质量为2.8克,则不符合催化剂的特点“只改变反应速率,而本身的质量和化学性质都不变”,故X一定不是该反应的催化剂,错误;C、根据质量守恒定律,反应前后元素的质量不变,可求2.2克丙烷(C3H8)中氢元素的质量=2.2g×![]() =0.4g,再求水中氢元素的质量=3.6g×
=0.4g,再求水中氢元素的质量=3.6g×![]() =0.4g,故X中不含有氢元素,正确;D、2.2克丙烷(C3H8)中碳元素的质量=2.2g-0.4g=1.8g,二氧化碳中碳元素的质量=2.2g×
=0.4g,故X中不含有氢元素,正确;D、2.2克丙烷(C3H8)中碳元素的质量=2.2g-0.4g=1.8g,二氧化碳中碳元素的质量=2.2g×![]() =0.6g,a中含有的碳元素是1.8g-0.6g=1.2g,而a的质量的2.8g,则a中一定会含有氧元素,错误。故选AC。
=0.6g,a中含有的碳元素是1.8g-0.6g=1.2g,而a的质量的2.8g,则a中一定会含有氧元素,错误。故选AC。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案【题目】(1)某化学兴趣小组的同学向无水乙醇中放入一小块金属钠,观察到有气泡产生。小组同学对这一现象产生了兴趣,进行了如下探究
(提出问题)无水乙醇和金属钠反应产生的气体是什么?
(查阅资料)I无水乙醇(CH3CH2OH)和金属钠反应生成乙醇钠CH3CH2ONa)和一种常见的可燃性气体;
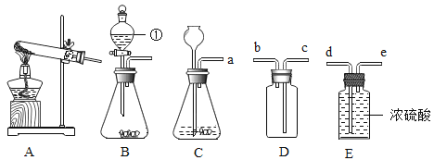
Ⅱ浓硫酸具有较强的吸水性,可用作某些气体的干燥剂,比
Ⅲ白色的无水硫酸铜粉末遇水后会变成蓝色。
(猜想与假设)猜想一:CO;猜想二:CH4;猜想三:H2。兴趣小组的同学提出上述猜想的理论依据是_______________
(设计并实验)兴趣小组的同学分成甲、乙两组设计实验方案进行探究。
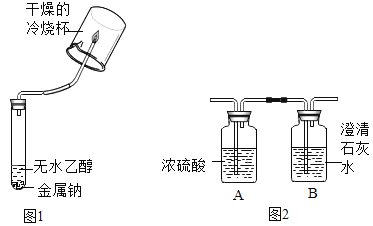
①甲组同学设计的实验方案如下:
实验操作 | 实验现象 | 实验结论 |
将反应产生的气体点燃在火焰上方罩一个干燥的冷烧杯 | 烧杯内壁有小液滴生成 | 猜想三成立 |
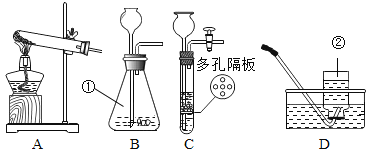
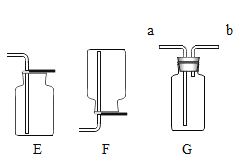
②乙组同学认为只完成上述实验猜想二也可能成立理由是 _________,并设计了如下实验进一步验证:将反应产生的气体点燃,燃烧产物依次通人A、B装置(如图2),测得A装置中质量增大,B装置中质量不变乙组的同学根据实验数据分析,证明猜想_________成立
(得出结论)无水乙醇与金属钠反应的化学方程式为_____________;该反应的基本反应类型是____________。
(实验反思)甲组同学受到乙组同学的启发认为只需要增加一个实验:再在火焰上方罩一个内壁蘸有澄清石灰水的烧杯,观察现象,就能使本组的实验方案更加完善。你认为此方案________ (选填“合理”或“不合理”)。
(拓展延伸)要确认该实验过程中所用的乙醇是无水乙醇的实验方法是____________。
(2)小明同学为了测定实验室中一瓶标签破损的硫酸的溶质质量分数,他取20g该硫酸于烧杯中,向其中加入10g锌粉(锌粉过量),完全反应后测得烧杯内物质的总质量为29.9g。该瓶硫酸的溶质质量分数是___________?