题目内容
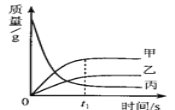
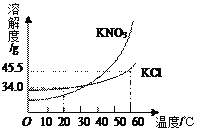
【题目】KNO3和KCl在不同温度时的溶解度曲线如图所示,下列说法正确的是
A. 温度低于40℃时,KNO3的溶解度一定小于KCl的溶解度
B. 将等质量的KNO3和KCl的饱和溶液从60℃降温到20℃,析出晶体的质量KNO3大于KCl
C. 将10℃时KNO3、KCl的饱和溶液升温至60℃,KNO3溶液中溶质的质量分数比KCl大
D. 将20℃时100gKCl的饱和溶液升温至60℃,需要再加入11.5gKCl固体才能使溶液恰好饱和
【答案】B
【解析】A、在30℃-40℃时,两条曲线有交点,此时KNO3的溶解度和KCl的溶解度相等,故错误;
B、将等质量的KNO3和KCl的饱和溶液从60℃降温到20℃,KNO3的溶解度比KCl的溶解度变化大,析出晶体的质量KNO3大于KCl,故正确;
C、将10℃时KNO3的溶解度大于KCl的溶解度,根据饱和溶液溶质的质量分数公式![]() 可知,将10℃时KNO3、KCl的饱和溶液溶质质量分数KCl大于KNO3,升温至60℃,KNO3、KCl的溶解度都增大,但溶液的成分都没有变化,KNO3溶液中溶质的质量分数比KCl小,故错误;
可知,将10℃时KNO3、KCl的饱和溶液溶质质量分数KCl大于KNO3,升温至60℃,KNO3、KCl的溶解度都增大,但溶液的成分都没有变化,KNO3溶液中溶质的质量分数比KCl小,故错误;
D、20℃时,KCl的溶解度为34.0g,60℃时,KCl的溶解度为45.5g,如果水为100g饱和溶液从20℃时升温至60℃,需要再加入11.5gKCl固体才能使溶液恰好饱和,但是题干中为100g溶液,故错误。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目