题目内容
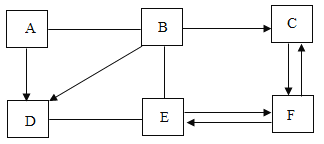
【题目】如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“﹣”表示相互能反应,部分反应物、生成物或反应条件已略去). 甲与A 溶液反应得到浅绿色溶液;A、B 发生中和反应,产物之一是厨房内常用的调味品;B、C 物质类别相同,且 C 的溶液与 D 的溶液反应可得到 B;乙与丙两种溶液反应生成两种不同颜色的沉淀.请回答:
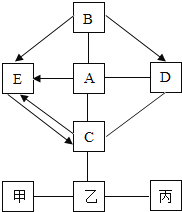
(1)B 化学式是_____;
(2)E→C 反应的化学方程式是_____.
【答案】NaOH ![]()
【解析】
根据A、B发生中和反应,产物之一是厨房内常用的调味品,推出A、B发生中和反应生成了氯化钠,所以可知A为盐酸,B为氢氧化钠,又因为A与甲可以反应生成浅绿色溶液,推出甲是铁, B、C类别相同,说明C为碱,C与D反应生成氢氧化钠,说明氢氧根离子来自于C,钠离子则来源于D,两者反应生成了氢氧化钠,而B氢氧化钠又可以生成D,可以推出D为碳酸钠,C与碳酸钠反应生成氢氧化钠,说明发生复分解反应,则需要C中另一个离子需要与碳酸根形成沉淀才可以保证复分解反应的发生,因此C为氢氧化钙,因此可以看出A为盐酸、B为氢氧化钠、C为氢氧化钙、D为碳酸钠,A能生成E,B也能生成E,酸和碱能生成的共同产物只有水,所以E为水,水与氧化钙反应生成氢氧化钙,氢氧化钙加热分解可以生成氧化钙和水,符合C与E相互转化关系,乙与丙反应生成两种不同颜色的沉淀,在初中常见有颜色沉淀为氢氧化铜蓝色沉淀、硫酸钡白色沉淀、碳酸钙白色沉淀以及氯化银白色沉淀,C为氢氧化钙,C与乙可以反应,甲为铁,可与乙反应,说明乙可与碱和金属单质反应,金属单质一般与酸、盐等发生置换反应,若乙为酸,则不能与丙生成两种沉淀,因此乙为盐,铁与盐发生置换反应,且能让乙与丙产生有色沉淀,则乙为含有铜的盐,丙则含有氢氧根离子,两种可以生成蓝色沉淀,同时还要有另一种颜色沉淀生成,则丙中除了氢氧根离子外,可以含有钡离子、钙离子,钡离子与硫酸根、碳酸根形成硫酸钡、碳酸钡沉淀,钙离子与碳酸根形成碳酸钙离子,但是乙和丙都是溶液,乙中含有铜,则排除碳酸根,所以乙为硫酸铜,丙含有氢氧根,与硫酸根形成白色沉淀,则丙为氢氧化钡,所以推出A为盐酸、B为氢氧化钠、C为氢氧化钙、D为碳酸钠、E为水、甲为铁、乙为硫酸铜、丙为氢氧化钡。
(1)根据分析可知B为氢氧化钠,化学式为NaOH;
(2)E为水,C为氢氧化钙,氧化钙与水反应生成氢氧化钙,所以E→C的反应化学方程式为![]() 。
。

【题目】为测定石灰石中碳酸钙的质量分数,小明取石灰石样品,加到足量的稀盐酸中,进行实验(假定样品中其他成分不与稀盐酸反应)。
石灰石样品的质量 | 烧杯和稀盐酸的总质量 | 反应后烧杯及烧杯中各物质的总质量 |
12.5g | 87.5g | 95.6g |
请计算:
(1)生成二氧化碳的质量______________。
(2)求样品中碳酸钙的质量分数________________(写出计算过程)
【题目】当空气中的CO2含量超过一定量时会影响人体健康。
[查阅资料]空气中CO2的体积分数为1%时,人会有心跳加快、困乏、注意力不集中、轻度恶心等症状;体积分数为5%时,会有呼吸不畅、头晕、耳鸣、血压升高等症状;体积分数为10%时,会有严重缺氧、丧失意识、昏迷等症状。
[提出问题]在没有专业测量仪器的情况下,如何检验空气中CO2的含量已经达到影响人体健康的程度?
[设计实验]依据CO2的性质,设计检验方法。
CO2性质 | 检验方法 | 预期现象 | |
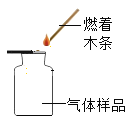
方法1 | (1) | 用燃着木条检验 | 燃着木条熄灭 |
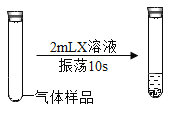
方法2 | 与水反应 | 用X溶液检验 | 溶液由紫色变为红色 |
方法3 | 与石灰水反应 | 用澄清石灰水检验 | 溶液中产生白色浑浊 |
(1)方法1依据的CO2性质是_______________。
(2)根据方法2的预期现象推断,所需试剂X是___________溶液。
(3)用化学方程式表示方法3的原理:_____________。
[配制样品]常温常压下,配制CO2体积分数不同的气体样品。
(4)收集5mLCO2与空气混合,得到500 mL 1%的气体样品;收集25 mL CO2与空气混合,得到500 mL_______%的气体样品。
[进行实验]常温常压下,集气瓶和试管中盛有空气或CO2气体样品,分别进行以下实验。
方法1 | 方法2 | 方法3 | |
实验过程 |
|
|
|
空气 | 正常燃烧 | 溶液无明显变化 | 溶液无明显变化 |
1%的CO2气体样品 | 正常燃烧 | 溶液无明显变化 | 溶液中产生白色浑浊 |
5%的CO2气体样品 | 正常燃烧 | 溶液由紫色变为红色 | 溶液中产生白色浑浊 |
[解释与应用]
(5)从灭火原理分析,方法1中均没有出现“燃着木条熄灭”的原因是________________。
(6)1班有部分同学在教室内出现“困乏、注意力不集中”等症状时,小林同学想用上述实验方法检测教室内CO2气体的含量,他应该选用的方法是__________(填方法序号)。
(7)2班小瑜同学收集了教室中的气体,尝试用方法2进行实验,发现溶液由紫色变为红色。由此现象推测此时教室中CO2的含量可能为___________(填字母序号)。
A1%以下 B1% C1%~ 5% D5%以上
【题目】阅读下面科普短文。
巧克力是极具营养价值的食品,某巧克力部分营养成分见下表。可可豆是制作巧克力的主原料,含水、单宁、可可脂等物质。制作巧克力时,可可豆发酵过程中减少了单宁的含量,从而降低了可可的苦味,同时生成二氧化碳、醋酸等物质。再通过精炼,让巧克力拥有滑顺的口感,通过去酸使巧克力透出清香,回火铸型后得到成型的巧克力。
可可脂是一种主要由三种脂肪酸构成的脂肪,熔点在 34~36℃,恰好低于口腔温度,但高于体表(手掌)温度。几种固体脂的融化曲线如图所示。
某巧克力的营养成分 |
项目 每 100 g |
热量 520 kJ 糖类 59.5 g 脂肪 31.93 g 蛋白质 5.78 g 钠 48 mg 钾 331 mg |

巧克力含有丰富的多源苯酚复合物,是防止心脏病的天然卫士。巧克力中的糖分还能起到缓解压力,消除抑郁情绪的作用。巧克力由于可可脂的特性,在夏天,表面会形成白色晶状物,类似白霜,影响观感,并不影响巧克力的质量,可放心食用。
依据文章内容回答下列问题。
(1)由表可知该巧克力中含量最高的营养素是_______________。
(2)可可豆发酵的过程属于_________(填“物理”或“化学”)变化。
(3)根据图可知,10℃时固体脂指数最小的是__________。
(4)解释巧克力“只融在口,不融在手”这句广告词中蕴含的科学原理________。
(5)下列说法正确的是_________。
A心脏病患者可适当食用巧克力
B巧克力中因含有单宁等物质使其略带苦味
C巧克力在口中能瞬间融化是因为其固体脂指数随温度变化大