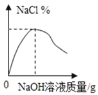
��Ŀ����
��ȤС���ͬѧ������ͭ�����ʽ���������̽�� ʵ��һ��������Ͷ������ͭ��Һ�У��������ɺ�ɫ�������ʵ�ͬʱ�������ݷų���
��������룩���������Ԫ�صĽǶȿ��ǣ��ų������������SO2��O2��H2�е�һ�ֻ� �֡�
���������ϣ������Ը��������Һ���Ϻ�ɫ��SO2��ʹ���Ը��������Һ��ɫ��
��O2+4KI+4HC1=2I2+4KC1+2HO��I2Ϊ�ⵥ�ʣ���������Һ������
��������ƣ������������룬���Ƿֱ���������·�����
(1)��ͬѧΪȷ���Ƿ��� SO2����������ͨ�����Ը��������Һ�У���Һ��ɫ δ�����仯�����������___SO2(��С����ޡ�)
(2)��ͬѧΪ�ж��Ƿ���O2��ͬʱȷ������ɷ֣��������ͼ1��ʵ��װ�á�
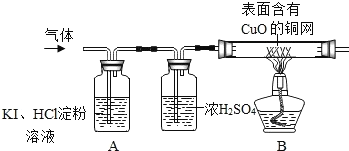
��ʵ����ۣ���ͼ װ�ã�A�й۲쵽____����֤���� O2��B �й۲쵽____֤���������� H2��
��ʵ�鷴˼�������Ϊ��ͬѧ�ڼ���֮ǰ��Ӧ��������____��ȷ����ȫ��
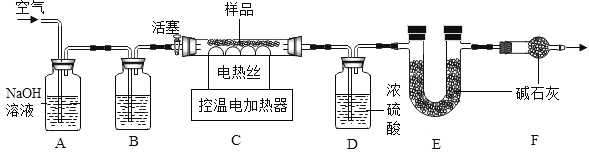
ʵ�������ȤС���ͬѧ�ֽ�һ������ Na2CO3��Һ���뵽 CuSO4��Һ�еõ�һ�ֻ�ѧʽ Ϊ aCuCO3?bCu(OH)2������ɫ�������� X����ͨ����ͼ��ʵ��װ�òⶨX����ɡ�
���������ϣ�Cu(OH)2��66��~68����ȫ�֡�������
Cu(OH)2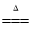 CuO��H2O��CuCO3��200��~220����ȫ�֡�������
CuO��H2O��CuCO3��200��~220����ȫ�֡�������
CuCO3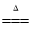 CuO��CO2������ʯ���������ƺ��������ƵĻ���
CuO��CO2������ʯ���������ƺ��������ƵĻ���
��ʵ�鲽�裩������������____��ȷ��ȡһ��������Ʒ X ���� C װ���У��ڴ�������һ��ʱ�����������װ�� D��E���������۹رջ��������� C װ���е��¶�Ϊ250���X�����ȷֽ⣬ֱ�� Cװ����ʣ������������ٱ仯Ϊ ֹ���ܴ�����___������ȴ�Ƶ�װ�� D����5.4g��װ�� E ���� 8.8g��
(3)ϴ��ƿ A������������Һ��������___��B����װҺ��Ϊ______��(������)
(4)ͨ������ɵã�a��b��_____��
(5)��ȱ��Fװ�ã���õ�a��b____��(ѡ�ƫ����ƫС����������)
(6)��һ���¶��£���һ������������ˮ�м���18.4g��ˮ����ͭ��ĩ(��ɫ)�� ��ֽ��貢���ˣ��õ�25g��ɫ����(CuSO4?5H2O)��һ����������Һ�������¶�����ˮ����ͭ���ܽ��Ϊ 40g������������ˮ��������___��(д���������)
�ⶨ��������Һ��pH�������������˽�����Ľ���״����һЩ��Һ�Ľ���pH���£�����Һ���У�������ǿ����( )
Һ�� | θҺ | ��Һ | ��֭ | Ѫ�� |
PH | 0.9��1.5 | 7.5��8.0 | 7.1��7.3 | 7.35��7.45 |
A. θҺ B. ��Һ C. ��֭ D. Ѫ��


 ��ȡҺ�� B.
��ȡҺ�� B.  ����ζ C.
����ζ C.  �㵹Һ�� D.
�㵹Һ�� D.  �������
�������