题目内容
【题目】氯化钠是人体不可缺少的物质,其主要作用是维持人体盐度平衡。
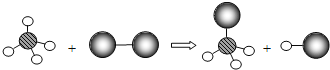
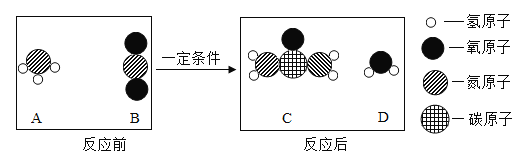
(1)下图为金属钠在氯气中燃烧生成氯化钠过程的示意图。
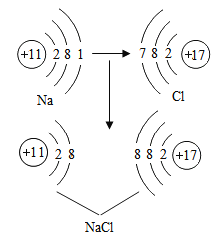
根据所给信息,请回答:
①钠原子在化学反应中易___(填“得到”或“失去”)电子.
②在化学反应前后,氯元素的化合价由_____变为______。
③依据原子的核外电子排布,将原子的最外层电子数相同元素归为同一族,将原子的核外电子层数相同的归为同一周期。氯元素和钠元素在元素周期表中位于同__(填“族”或“周期”)
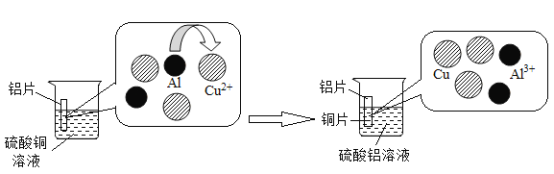
(2)用海水晒盐、盐湖水煮盐,这样制得的食盐还有泥沙、氯化镁、氯化钙、硫酸钠杂质,称为粗盐。粗盐经过处理可制得精一盐。流程如下:
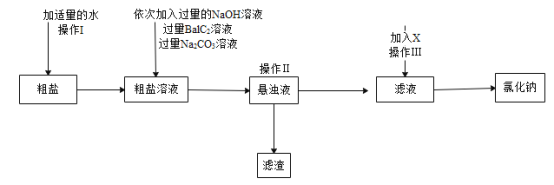
①实验室中进行操作Ⅰ时用到玻璃棒搅拌,其搅拌的目的是 ____。
②加入的试剂X的是___。
③通过操作Ⅱ所得滤渣中除了泥沙和Mg(OH)2、BaSO4、CaCO3,还有__(用化学式表示)。
【答案】失去 0 -1 周期 加快粗盐的溶解 稀盐酸 BaCO3
【解析】
(1)①由原子结构示意图可知,钠原子的最外层电子数是1;在化学反应中易失去电子;
②反应前氯气中氯元素的化合价为0;反应后氯化钠中钠元素的化合价为+1价,设氯化钠中氯元素的化合价为x,则(+1)+x=0,解得x=-1价;
③据图可知,氯原子和钠原子的电子层数都是3,氯元素和钠元素位于同一周期;
(2)①实验室中进行操作Ⅰ是溶解,用到玻璃棒搅拌,其搅拌的目的是加快粗盐的溶解;
②步骤Ⅲ中所加试剂X是稀盐酸,用来除去过量的氢氧化钠和碳酸钠;
③过量氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,过量氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,过量碳酸钠分别和氯化钙、氯化钡反应生成碳酸钙沉淀、碳酸钡沉淀和氯化钠,所以操作Ⅱ所得滤渣中还有碳酸钡,化学式为BaCO3。

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应。
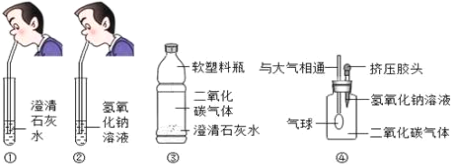
同学们在吹气后观察到①中澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象。观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用________,针对②中的情况,师生共同开始探究之旅。
(提出问题)二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
(猜想假设)猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应。
(实验探究)
Ⅰ:小明设计了如图所示的③、④两个实验。
实验现象:③中的软塑料瓶________________,④中气球膨胀。
II:小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是___________。
III:小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
取④实验后的溶液少许,再向其中加入____________。 | _________ | 验证了二氧化碳和氢氧化钠溶液反应。 |
(实验结论)二氧化碳和氢氧化钠溶液发生了化学反应。
(反思拓展)实验②中反应后所得溶液中溶质成分:猜想(1):只有碳酸钠;猜想(2):__________。
(数据处理)
小明将实验③中浑浊的液体进行_______(填操作名称)、洗涤、烘干,称量所得固体质量为1.0g。试计算:实验③中参加反应的二氧化碳的质量为____________克?(列式计算)