题目内容
【题目】贵州有丰富的溶洞旅游资源,溶洞的形成是二氧化碳循环的结果。在自然界中,溶有二氧化碳的雨水,会使石灰石构成的岩层部分溶解,使碳酸钙转变成可溶性的碳酸氢钙,其发生的变化为![]() 。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为
。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为![]() 。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。
。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。

请结合文本回答问题:
(1)岩层部分溶解时,发生的化学变化的基本类型为_____;
(2)经测定某溶洞中的水为硬水,其原因可能是_____;
(3)洞区居民使用的水壶内常形成一种白色垢状物,可用稀盐酸除去,其原因是_____;
(4)不能随意进入溶洞的原因是_____;
(5)请写出一种自然界中二氧化碳的消耗途径_____。
【答案】化合反应(填化合也可) 溶有较多碳酸氢钙[或CaCO3+CO2+H2O=Ca(HCO3)2,合理即可] 白色垢状物主要成分碳酸钙与盐酸反应而溶解(或CaCO3+2HCl=CaCl2+ CO2↑+H2O,合理即可) 溶洞中CO2含量较高对人体健康有害(合理即可) 光合作用[或 CO2与水(海水)反应,合理即可]
【解析】
(1)石灰石构成的岩层部分溶解,使碳酸钙转变成可溶性的碳酸氢钙,其发生的变化为CaCO3+CO2+H2O=Ca(HCO3)2,该反应符合“多变一”的特点,故该反应为化合反应;
(2)经测定某溶洞中的水为硬水,其原因可能是:该水中溶有较多碳酸氢钙[或CaCO3+CO2+H2O=Ca(HCO3)2,合理即可];
(3)洞区居民使用的水为硬水,水中溶有较多碳酸氢钙。碳酸氢钙在加热条件下生成碳酸钙,故壶内形成的白色垢状物主要为碳酸钙,可用稀盐酸除去,其原因是:白色垢状物的主要成分碳酸钙与盐酸反应而溶解或CaCO3+2HCl=CaCl2+ CO2↑+H2O;
(4)不能随意进入溶洞的原因是水中的碳酸氢钙会分解析出碳酸钙沉淀和二氧化碳、水,溶洞中CO2含量较高对人体健康有害;
(5)自然界中二氧化碳的主要消耗途径之一为植物的光合作用或 CO2与水(海水)反应。

【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1-2.5g进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4=CuSO4+H2O+Cu
(进行实验)
实验1:收质量比1:11的木炭粉和氧化铜混合物1.2g,进行实验。
序号 | 1-1 | 1-2 |
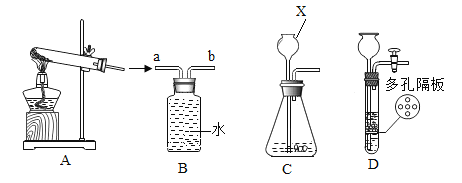
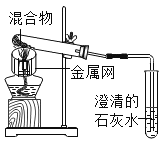
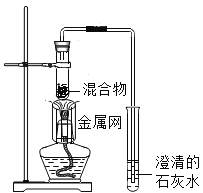
装置 |
|
|
反应后物质的款色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1-2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2-1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2-2 | 1:10 | 混有很少量黑色物质 | |
2-3 | 1:11 | 混有极少量黑色物质 | |
2-4 | 1:12 | 无黑色物质 | |
2-5 | 1:13 | 混有较多黑色物质 | |
(1)木碳还原氧化铜的化学方程式:_____。
(2)实验1-2中,证明生成CO2的现象是_____。
(3)实验1的目的是______。
(4)实验2的结论是______。
(反思与评价)
(5)实验2没有进行质量比为1:14的实验,理由是____。
(6)为检验2-4的红色固体中是否含Cu2O,所需试剂是______。
【题目】某实验室为了测定石灰石样品中碳酸钙的含量,进行如下实验:
步骤 1:称取 40g 石灰石样品(假设杂质耐高温且不与酸反应),高温煅烧一段时间,恢复到室温,测得固体质量减少了11g。
步骤 2:向剩余固体中加入足量的稀盐酸至不再反应为止,生成气体的质量与时间的关系如下表:
时间 | t0 | t1 | t2 | t3 | t4 | t5 | t6 | t7 |
气体/g | 0 | 1.5 | 2.8 | 3.7 | 4.2 | 4.3 | 4.4 | 4.4 |
(1)步骤1中生成二氧化碳的质量为_____g。
(2)求步骤1中生成的氧化钙的质量_____(写出计算过程)。
(3)根据步骤2数据画出生成气体的质量与时间的关系_____。

(4)样品中碳酸钙的质量分数_____。(保留到 0.1%)