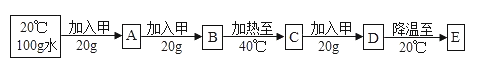
��Ŀ����
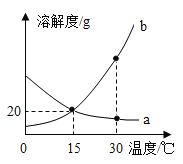
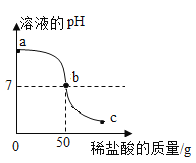
����Ŀ��ij������Ʒ�к�������NaCl��Ϊ�ⶨ����Ʒ��Na2CO3��������������ȡ������Ʒ15g������������ϡ���ᣬ��ͼ�Dz������������������ϡ���������Ĺ�ϵͼ��
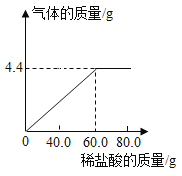
(1)��Ʒ��Na2CO3������������__��
(2)ǡ�÷�Ӧ��������Һ�����ʵ���������___��(д��������̣��������һλС��)
(3)������ϡ����80.0gʱ��������Һ��Na+������Ϊ__��(�������һλС��)
���𰸡���1��70.7%
��2��22.8%���������)
��3��6.3g
��������
������4.4g������̼��Ҫ��̼���Ƶ�����Ϊx�����ɵ��Ȼ��Ƶ�����Ϊy��
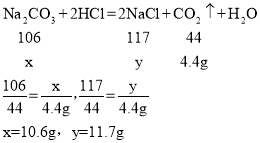
��Ʒ��̼���Ƶ���������Ϊ![]()
������Һ���Ȼ��Ƶ�����Ϊ11.7g+(15g��10.6g)=16.1g
ǡ�÷�Ӧ������Һ���Ȼ��Ƶ���������Ϊ![]() ��
��
������ϡ����80.0gʱ�����к��е������ӵ�����Ϊ![]() ��
��
��(1)��Ʒ��Na2CO3������������70.7%��
(2)ǡ�÷�Ӧ��������Һ�����ʵ���������Ϊ22.8%��
(3)������ϡ����80.0gʱ��������Һ��Na+������Ϊ6.3g��

 �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�����Ŀ��ij��ȤС��ͬѧ����ͼ1װ����ȡ���岢̽�������ijЩ����.
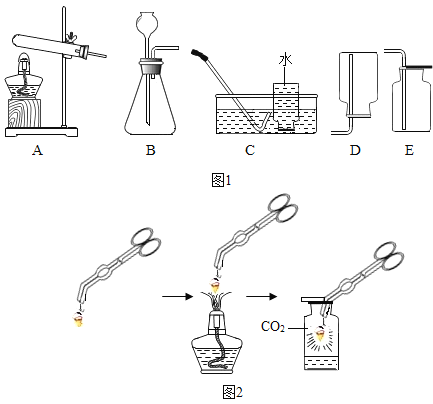
��1����ȡ����
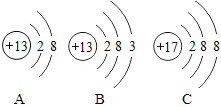
����ѡ��A��C�����ȡ��������Ӧ�Ļ�ѧ����ʽΪ__��
����ʯ��ʯ��ϡ������ȡCO2�Ļ�ѧ����ʽΪ__��ѡ�õķ������ռ�װ����__�����ţ������Ӻ�װ�ã���ҩƷ����װ��ǰӦ���еIJ�����__��
��2��̽�����������
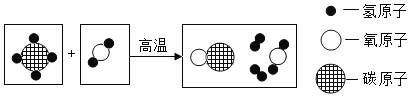
ijͬѧ�ڿ����е�ȼþ����������CO2��Ϩ��ȼ�յ�þ�����������þ���ڳ���CO2�ļ���ƿ��û��Ϩ������ȼ�գ�����ƿ�ڱڳ��ֺ�ɫ���壬ƿ�׳��ְ�ɫ���壬ʵ�������ͼ2��ʾ����ش�
�ټг�þ��������������__��
�����ɵĺ�ɫ������__��д��ѧʽ����
�۲������ϣ�MgO��Mg��OH��2��MgCO3��Ϊ������ˮ�İ�ɫ���壮ͬѧ���ۺ���Ϊ��ɫ���岻������Mg��OH��2��������__��
��Ϊ��һ��ȷ����ɫ����ijɷ֣���������ʵ�飺
ʵ����� | ʵ������ | ʵ����� |
ȡ��ɫ�������Թ��У���������ϡ���� | __ | ��ɫ���岻��MgCO3������MgO |
��þ��CO2��ȼ�յĻ�ѧ����ʽΪ__��ͨ������̽�������ȼ�ջ���������ʶ��__��