题目内容
【题目】为得到高纯度碳酸钙,实验室用Na2CO3溶液与CaCl2溶液反应制取。现将150gCaCl2溶液分四次加入盛有100gNa2CO3溶液的烧杯中,充分反应,四次测量所得数据见下表:
次数 | 第一次 | 第二次 | 第三次 | 第四次 |
累计加入CaCl2溶液的质量/g | 40 | 80 | 120 | 150 |
烧杯中溶液的总质量/g | 134 | 168 | 202 | 232 |
(1)第___________次恰好完全反应,此时生成沉淀的总质量为___________g。
(2)第四次测量时,所得溶液中的溶质有___________(填化学式)。
(3)CaCl2溶液的溶质的质量分数为___________。(写出计算过程)
【答案】三 18 NaCl、Ca2Cl 16.65%
【解析】
根据第一次烧杯中溶液总质量减少100g+40g-134g=6g,第二次烧杯中溶液总质量减少100g+80g-168g=12g,第三次烧杯中溶液总质量减少100g+120g-202g=18g,第四次烧杯中溶液总质量减少100g+150g-232g=18g,分析可知即第三次恰好完全反应,则第四次加入氯化钙溶液过量;根据前三次都可以计算出氯化钙溶液的溶质的质量分数。
(1)根据四次实验总质量的减少量知,第三次恰好完全反应,此时生成沉淀的质量为:100g+120g-202g=18g,故填:三,18。
(2)第四次测量时,氯化钙溶液过量,可知溶液中有Na2CO3溶液与CaCl2溶液反应生成的NaCl,以及加入过量的CaCl2溶液,因此含有的溶质为NaCl和CaCl2,故填:NaCl、CaCl2。
(3)由表可知第一次加入40g氯化钙溶液,生成碳酸钙沉淀的质量为100g+40g-134g=6g。设40g氯化钙溶液中溶质的质量为x;
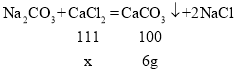
![]()
x=6.66g
则氯化钙溶液的溶质的质量分数为:![]()
答:氯化钙溶液的溶质质量分数为16.65%。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】阅读下面科普短文。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。

表1鲜土豆中主要营养物质的含量(每100g)
蛋白质/g | 脂肪/g | 淀粉/g | 钙/mg | 磷/mg | 维生素C/mg |
1.5~2.3 | 0.4~0.94 | 17.5~28.0 | 11~60 | 15~68 | 20~40 |
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:

土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。
依据文章内容回答下列问题。
(1)表1中的“钙”指的是________(填“元素”或“原子”)。
(2)由图1可知:60min内,______(填序号)。
A浸泡30min比10min脆性分值高
B浸泡10min,硬度、咬碎感均无明显变化
C随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图2可知:土豆片的淀粉含量与浸泡时间的关系是________________。
(4)変绿、发芽的土豆不宜食用,其原因是___________________。
(5)下列说法不正确的是____(填序号)。
A土豆是四大粮食作物之一 B土豆中维生素C含量最高
C用水泡可防止土豆片褐変 D土豆开发应用的前景广阔