��Ŀ����
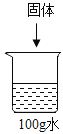
����Ŀ��ij��ȤС���ڳ��º�������ͬ�����£���10.00g�������ʷֱ�������ͬ�����ձ��������ڷ����ڿ����У��ձ�������������ʱ��仯���±�����ش��������⡣
ʱ�� | ����/g | |||||
ˮ | ����ʯ��ˮ | ϡ���� | Ũ���� | �Ȼ���Ũ��Һ | �Ȼ���Ũ��Һ | |
1�� | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2�� | 5.76 | 5.94 | 6.69 | 12.25 | 8.47 | 10.33 |
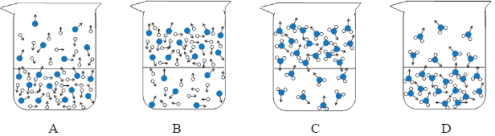
(1)����ͼʾ�ܷ�ӳˮ�ڿ����з���ʱ�����仯����ʾ��ͼ��______(����ĸ���)��ͼ��![]() ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�![]() ��ʾ��ԭ��
��ʾ��ԭ��
(2)Ϊ����һ�ְ�ȫ�������ij�ʪ������ѡ���ϱ��е�(�����ʵĻ�ѧʽ)____��
(3)������100g 20%��ϡ���ᣬ����Ҫ��������Ϊ98%(�ܶ�Ϊ1.84g/cm3)��Ũ����____ml��(�����������)
(4)Ϊ��һ���о�ϡ���᳨�ھ��ú�Ũ�ȱ仯�����м�ͬѧ����ϡ����Ũ�ȿ��ܻ���������_____��
���𰸡�D CaCl2 11 ϡ�������ܼ�ˮ�����������������Ȼ�������Ļӷ���
��������
ˮ����ʱ��Һ�����ϵ�λ�����ˮ���Ӹ���Ӧ��С��Һ�����µ�λ�����ˮ���Ӹ�������������Ӽ�ļ������Һ����Ӽ�ļ����
��1��ˮ����ʱ��Һ�����ϵ�λ�����ˮ���Ӹ���Ӧ��С��Һ�����µ�λ�����ˮ���Ӹ�������������Ӽ�ļ������Һ����Ӽ�ļ������ͼʾ�ܷ�ӳˮ�ڿ����з���ʱ�����仯����ʾ��ͼ��D��
��2���Ȼ�����Һ�����ԣ�������ˮ���������������������Ũ������Ȼ������ˮ�ԣ�����ǿ��ʴ�ԣ�����ʯ��ˮ��ϡ���ᡢ�Ȼ��Ʊ�����Һ����������ˮ�ԣ�����һ�ְ�ȫ�������ij�ʪ������ѡ���ϱ��е�CaCl2��
��3������100g 20%��ϡ���ᣬ��Ҫ��������Ϊ98%���ܶ�Ϊ1.84g/cm3����Ũ�������Ϊx������100g��20%=x��1.84g/cm3��98%��x��11cm3����11mL������������Ϊ98%���ܶ�Ϊ1.84g/cm3����Ũ�������Ϊ11mL��
��4��Ϊ��һ���о�ϡ���᳨�ھ��ú�Ũ�ȱ仯�����м�ͬѧ����ϡ����Ũ�ȿ��ܻ���������ϡ�������ܼ�ˮ�����������������Ȼ�������Ļӷ�����

 �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�����Ŀ���ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ�����ᷢչ��Ƽ����������˾��ס��ϳɰ����յ���Ҫ�������£�
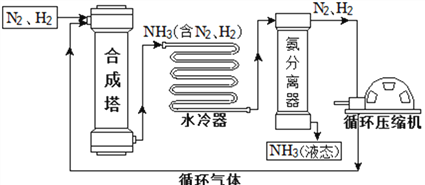
(1)�ϳ����еķ�Ӧ�����ڸ��¡���ѹ�����������½��У��÷�Ӧ�ķ��ű���ʽ�ǣ�__________________________________________________��
(2)���������п��ظ�ʹ�õ�������_______________(�ѧʽ)��
(3)���ݱ��е����ݻش����⡣
���� | H2 | N2 | O2 | NH3 |
�е�/��(1.01��105 Pa) | �C252 | �C195.8 | �C183 | �C33.35 |
��1.01��105 Paʱ��Ҫ������NH3��N2��H2���뿪���������˵��¶�Ӧ�ÿ�����______����
(4)��ͼ�Ǻϳ����з�����Ӧ��������ʾ��ͼ��
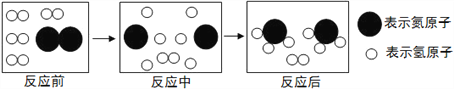
��ͼ��֪���ַ�Ӧ��N2��H2�ķ��Ӹ�����Ϊ____���÷�Ӧ�е���С������_________(��д��ѧ����)��
����Ŀ����֪��20��ʱ��NaCl��NaNO3���ܽ�ȷֱ�Ϊ36 g��88 g��
| ��� | �� | �� | �� | �� | �� |
�������� | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
���������/g | 30 | 60 | 30 | 60 | 90 | |
ˮ������/g | 100 | 100 | 100 | 100 | 100 |
�ϱ���20��ʱʵ��ó������ݣ����ݸ����ݣ������й��ڢ١���������Һ��˵������ȷ����
A. ������������=��B. ��Һ������ ��<��
C. ����������������=��D. �����������ܼ���������Ϊ22:25