题目内容
【题目】MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
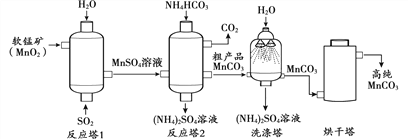
(1)反应塔1中的反应为:MnO2+SO2==MnSO4,其中化合价发生改变的元素是________。
(2)洗涤塔中喷水的目的是__________。
(3)烘干塔中需选择“低温”干燥的原因是_______________。
(4)上述流程中的产品除高纯MnCO3外,还有______________。
【答案】 Mn、S 除去粗产品MnCO3中的(NH4)2SO4 防止MnCO3高温分解 (NH4)2SO4溶液、CO2
【解析】(1)反应前锰元素的化合价是+4,反应后锰元素的化合价是+2,反应前硫元素的化合价是+4,反应后硫元素的化合价是+6。(2)MnCO3不溶于水,而(NH4)2SO4易溶于水,所以洗涤塔中喷水的目的是除去粗产品MnCO3中的(NH4)2SO4。(3)烘干塔中需选择“低温”干燥的原因是防止MnCO3高温分解。(4)根据流程示意图,上述流程中的产品除高纯MnCO3外,还有(NH4)2SO4溶液、CO2。

练习册系列答案
相关题目