题目内容
【题目】根据下列实验装置图,回答问题。
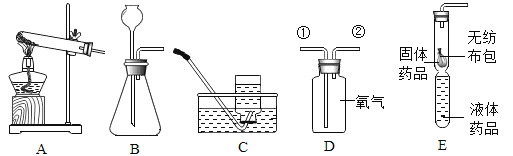
(1)实验室里用A装置加热高锰酸钾(KMnO4)制取氧气时,发生装置在加入药品前,应该进行的操作是_____。
(2)用装置C收集氧气时,所得氧气不纯的原因是_____(写出一点)。
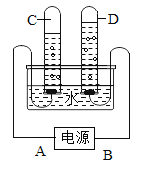
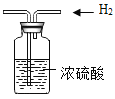
(3)若将D装置中的氧气从瓶内排出,水应从_____(填“①”或“②”)通入。
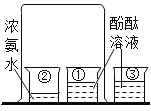
(4)装置E是用软塑料管自制的气体发生装置,利用该装置制取氧气时,液体药品是_____。
(5)小易同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,小宇同学发现用排水法收集到的O2大于理论产量。针对这一现象,小易和小宇同学进行了如下探究:
(提出猜想)猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2
(实验验证)小易和小宇分成两组,分别进行下列实验:
小易同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想_____错误。
小宇同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论,小宇同学选择的实验方法是_____。
【答案】检查装置气密性 导管口未出现连续均匀气泡时,进行了氧气的收集(答案合理即可) ① 过氧化氢溶液 I和III 观察带火星的木条是否复燃
【解析】
(1)有气体参与的反应,实验开始前应先检查装置气密性;
(2)排水法收集氧气时,刚开始出现气泡时,是内部受热膨胀鼓出的空气,氧气含量较低,若一出现气泡进行收集,则得到氧气不纯(答案合理即可);
(3)水的密度大于氧气,且氧气不易溶于水,从①处进水,水在底部,将其上部的氧气从②处排出,达到排出氧气的目的;
(4)装置为固液不加热型,所以选用过氧化氢溶液加入二氧化锰催化分解制取氧气,液体药品为过氧化氢溶液;
(5)小易称量二氧化锰反应前后质量不变,说明没有生成物生成,所以不是二氧化锰分解生成氧气,因此猜想中带有二氧化锰的都不对,所以猜想I和III都不对;可以利用氧气可以使带火星的木条复燃的性质判断猜想II的正确性,将带火星的木条靠近锰酸钾加热产生的气体附近,木条复燃,则证明生成了氧气。

【题目】某学习小组的同学对过氧化氢分解进行探究。
Ⅰ、(探究一)影响过氧化氢分解快慢的因素
分别取5mL过氧化氢溶液进行实验,测定产生4mL氧气所需时间,实验结果记录如下:
实验序号 | 过氧化氢溶液的浓度% | 温度℃ | 二氧化锰粉末用量/g | 反应时间 |
① | 30 | 35 | 0 | t1 |
② | 30 | 55 | 0 | t2 |
③ | 5 | 20 | 0.1 | 3s |
④ | 15 | 20 | 0.1 | 1s |
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1_____t2(填“>”、 “=”或“<”)
(2)能说明过氧化氢分解快慢与过氧化氢溶液的浓度有关的实验是_______(填实验序号),合理的结论是____________。
交流探讨:二氧化锰属于金属氧化物,其它金属氧化物能否起到类似二氧化锰的催化作用?
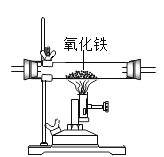
Ⅱ、(探究二)探究氧化铁是否对过氧化氢分解起催化作用
操作步骤 | 实验情况记录 | 结论 | |
① |
| A试管上方带火星的木条未复燃 B中出现气泡快,带火星的木条复燃 | 氧化铁_______(填“不影响”、“减慢”或“加快”)过氧化氢分解 |
② | 将B试管中的混合物过滤,把滤渣烘干、称量。 | 固体质量为________ | 氧化铁质量不变 |
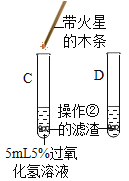
③ |
| C试管上方带火星的木条________, D中溶液变成黄色 | 氧化铁可作过氧化氢分解的催化剂 |
得出结论:过氧化氢分解快慢受______________________________等因素影响。