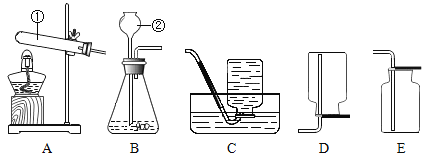
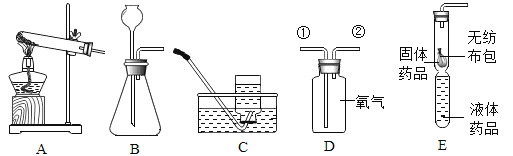
题目内容
【题目】竹炭包是一种集观赏与空气净化为一体的产品,这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行吸附,某课外小组对竹炭进行初步探究。
(提出问题)竹炭中是否含有碳元素
(猜想与假设)竹炭中含有碳元素
(查阅资料)①新鲜的鸡血,遇一氧化碳由鲜红变为暗红②氢氧化钠能与二氧化碳发生化学反应
(设计实验)通过检验竹炭燃烧产物,证明竹炭中含有碳元素,所用装置如下图所示:(A装置的作用为吸收空气中的水和二氧化碳)
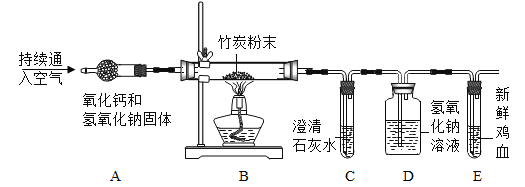
(1)实验开始后,C装置中产生白色沉淀,反应化学方程式为____________________________,E装置中新鲜的鸡血变为暗红色,证明______________________。
(2)小红认为应在A、B装置间再增加一个C装置,目的是______________________。
(3)小兵认为该实验设计中还存在着一个明显的缺点,该缺点是__________________,改进方法是_________________________________。
(4)小明认为能用图所示的装置替换原装置中的E装置,你认为_________________(填“可以”或“不可以”),原因是__________________________。
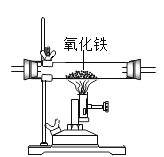
(结论)竹炭中含有碳元素
9.某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示:求:
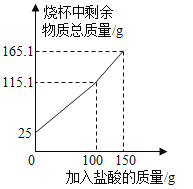
(1)产生CO2的总质量为_________g。
(2)鸡蛋壳中碳酸钙的质量分数____________。
【答案】CO2 + Ca(OH)2=CaCO3 ↓+ H2O 装置B中有一氧化碳生成 检验二氧化碳是否除尽 尾气中一氧化碳有毒,污染空气 要在结尾处加装酒精灯点燃一氧化碳 不可以 通入E装置中的气体除了有一氧化碳外还有氧气,加热有可能会发生爆炸 9.9g 90%
【解析】
(1)装置C中氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,反应方程式为:CO2 + Ca(OH)2=CaCO3 ↓+ H2O;E装置中新鲜的鸡血变为暗红色,说明装置B中有一氧化碳生成。
(2)为了防止空气中的二氧化碳影响实验,故要在AB间装C装置,检验二氧化碳是否除尽。
(3)该反应中有一氧化碳生成,缺少尾气处理装置,一氧化碳有毒,污染空气,故要在结尾处加装酒精灯点燃一氧化碳。
(4)通入E装置中的气体除了有一氧化碳外还有氧气,加热有可能会发生爆炸,故,不可以。
9.(1)由质量守恒定律可知,生成二氧化碳的质量为:25g+150g-165.1g=9.9g
(2)设生成9.9g的二氧化碳需要碳酸钙的质量为x
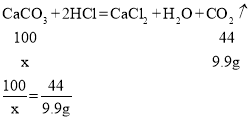
解得x=22.5g
故样品中碳酸钙的质量分数为:22.5g÷25g×100%=90%。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】下列知识归纳,完全正确的一组是
A.能量变化 | B.环境保护 |
①电解水是将电能转化成化学能 ②溶解过程中有的吸热,有的放热 ③在化学反应中只有燃烧才能放出热量 | ①小区设置废旧电池回收箱 ②重复使用塑料袋和塑料盒 ③工业“三废”处理达标后排放 |
C.数字含义 | D.资源节约 |
①Fe2+:一个亚铁离子带2个单位正电荷 ②SO3:一个三氧化硫分子中含有3个原子 ③ | ①废旧金属回收利用 ②提倡使用乙醇汽油 ③实验后用剩药品放回原瓶 |
A.AB.BC.CD.D
【题目】为测定4.24g某变质氢氧化钠固体中碳酸钠的质量分数,将其配置成100mL溶液,分成两等分,用如下两种方法进行测定。
加入的试剂 | 测得数据 | |
方法1 | 足量 | 碳酸钡沉淀1.97g |
方法2 | 足量 | 二氧化碳气体0.44g |
请完成上述表格,并自主选择一种方法,计算出样品中碳酸钠的质量分数。