题目内容
【题目】已知在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。已知氢氧化钠溶液可吸收二氧化碳气体,某化学课外兴趣小组对生成物中碳的氧化物种类进行如下探究:
(提出问题)生成物中有哪几种碳的氧化物?
(设计实验)依据CO和CO2的性质,兴趣小组同学设计了如下实验:
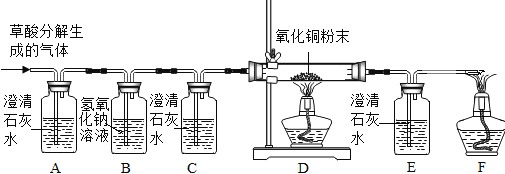
(实验探究)
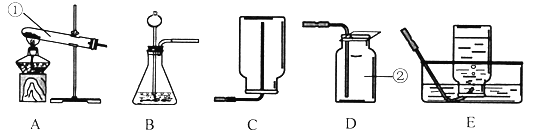
(1)观察到_____装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。该反应的化学方程式为_____。
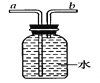
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO,分别是:①D装置中出现_____的现象;②_____。
(实验结论)通过实验探究证明:生成物中有CO和CO2两种气体。
(问题讨论)
(3)C装置的作用是_____,装置末端酒精灯的作用是_____。
(4)如D装置中硬质玻璃管(含药品)实验前质量为112.5g,实验后质量为109.3g,则参与反应的氧化铜质量为_____g。
【答案】A CO2+Ca(OH)2=CaCO3↓+H2O 黑色固体粉末变成红色 E装置中的石灰水变浑浊 验证二氧化碳是否除尽,排除对一氧化碳检验的干扰 点燃尾气中的一氧化碳,防止污染空气 16
【解析】
[实验探究]
(1)观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.二氧化碳和石灰水反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO,分别是:
①D装置中出现:黑色粉末变成红色粉末;
②C中石灰水不变浑浊,F中石灰水变浑浊。
[问题讨论]
(3)B装置的作用是吸收二氧化碳,C装置的作用是检验二氧化碳是否被完全吸收;装置末端酒精灯的作用是:把一氧化碳转化成二氧化碳,防止污染环境.
(4)如E装置中硬质玻璃管(含药品)实验前质量为112.5g,实验后质量为109.3g,则反应的氧化铜中氧元素质量为:112.5g-109.3g=3.2g,则参与反应的氧化铜质量为:3.2g÷![]() ×100%=16g。
×100%=16g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案