题目内容
【题目】生铁是铁和碳的合金.为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入65.0g稀硫酸,恰好完全反应(假设杂质不参与反应).测得的实验数据如下:
反应前 | 反应后 | |
烧杯及其中物质的质量 | 97.0g | 96.8g |
请你完成有关计算(结果保留一位小数):
(1)反应放出的氢气是多少?
(2)生铁样品中铁的质量分数是多少?
(3)反应后所得溶液的质量是多少?
【答案】(1)0.2g,(2)93.3%,(3)70.4g
【解析】
解:(1)根据质量守恒定律,反应生成的氢气质量=97g﹣96.8g=0.2g
(2)设生铁中铁的质量为x
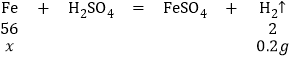
56:2=x:0.2g
x=5.6g
生铁样品中铁的质量分数=![]() ×100%=93.3%
×100%=93.3%
(3)反应后所得溶液的质量为:5.6g+65.0g﹣0.2g=70.4g.
答:(1)生成氢气0.2g,
(2)生铁中铁的质量分数为93.3%,
(3)反应所得溶液的质量为70.4g.

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案【题目】一次用餐中,小丽同学对“固体酒精”产生好奇,于是她决定买回一袋,对其进行研究.
(收集资料)通过阅读标签及查阅资料,她获得如下信息:
(1)该固体酒精中含有酒精、氢氧化钠等物质.
(2)酒精的化学式为C2H5OH
(提出问题)
(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是不是显碱性?请同学们帮小丽同学从下面试剂中选择合适试剂进行鉴别_____(填序号)
A硫酸铜 B氯化钠 C硝酸钾 D酚酞
(2)固体酒精中的氢氧化钠是否变质及变质的程度如何?
(猜想)
猜想一:没有变质,只含有氢氧化钠
猜想二:全部变质,只含有碳酸钠
猜想三:部分变质,含有________
请写出氢氧化钠在空气中变质的化学方程式____________.
(实验探究)取了少量固体酒精溶于足量水,充分溶解并过滤,取少量上述滤液于试管中,滴入几滴无色酚酞溶液,液体呈红色,甲同学认为固体中含有氢氧化钠,乙同学认为甲同学的结论不正确,其理由是______________________________.
(实验探究)于是小丽同学和同学们经过讨论并请教老师后,进行了实验探究.请帮她完成下面实验报告(写出详细步骤)
实验操作 | 实验现象 | 实验结论 |
__________ | 有气泡产生 | 猜想一不成立 |
再取少量滤液于试管加入过量的氯化钙溶液,充分 反应后,再加入_____ | 有白色沉淀产生, 溶液_____ | 则猜想_____成立 |
(拓展应用)除去部分变质的氢氧化钠溶液中的杂质,方法是_________(用化学方程式表示).
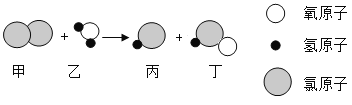
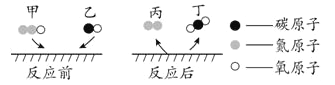
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。甲、乙、丙、丁表示四种物质,它们的部分化学式和微观示意图分别列于下表:
物质 | 甲 | 乙 | 丙 | 丁 | 图例: |
化学式 | H2O | C | ? | H2 | |
微观示意图 |
|
|
| ? |
(1)请你画出丁物质的微观示意图_________。
(2)构成甲物质的粒子是_________。
(3)四种物质中属于氧化物的是______、______(填化学式),请你从微观角度描述判断的依据:_______。