��Ŀ����
A�����������װ��ͼ���ش��й����⣺

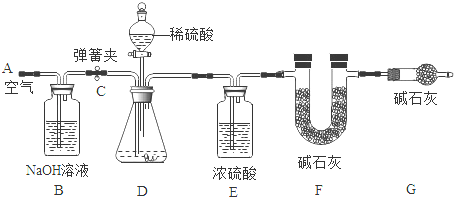
��1��д��װ��ͼ�б�����������ƣ�a ��b ��
��2��д��ʵ�����ô���ʯ��ϡ���ᷴӦ��ȡ������̼�Ļ�ѧ����ʽ ����ѡ�õ��ռ�װ���� (����ĸ)��ijͬѧ��̼���Ʒ�ĩ��ϡ���ᷴӦ����ȡ������̼��Ϊ�˽Ϻõؿ��Ʒ�Ӧ���ʣ���ѡ�õķ���װ���� (����ĸ)��
B��ij��ѧ��ȤС���ѧ�������ֽ���R���ڳ���ѧ���Ľ������˳����У���С��Ϊ���˽�R�볣����������ͭ�Ľ������˳��������̽�����
���������롿���ǿ��ǵ����Ļ�Ա�ͭǿ�������ֽ����Ļ��˳���������²��룺
����һ��Al��Cu��R��������� ����������R�� Al��Cu��
���������ϡ� R��һ������ɫ�Ľ�������R������Һ��ֻ��+2��R������Һ����ɫ�����������ı�����γ�һ�����ܵ�����Ĥ�����������Ȼ���������������Һ��Ϊ��ɫ��
��ʵ��̽����Ϊ��̽����һ�ֲ���������ס��ҡ�����λͬѧ�ֱ���Բ���һ������������������ʵ�鷽����չ��ʵ��̽����
��������˼��
�������ֲ����������λͬѧ�����۽��������ֱ�ͬѧ��ʵ��ǰû�д�ĥ��˿������ܻᵼ��ʵ����۴������������ȴ�ĥ��˿���ٽ�����뵽��ͬѧ��ʵ���ù�����Һ�У�һ��ʱ�����Һ����ɫ ������ȷ�ϲ������������������������

��1��д��װ��ͼ�б�����������ƣ�a ��b ��
��2��д��ʵ�����ô���ʯ��ϡ���ᷴӦ��ȡ������̼�Ļ�ѧ����ʽ ����ѡ�õ��ռ�װ���� (����ĸ)��ijͬѧ��̼���Ʒ�ĩ��ϡ���ᷴӦ����ȡ������̼��Ϊ�˽Ϻõؿ��Ʒ�Ӧ���ʣ���ѡ�õķ���װ���� (����ĸ)��
B��ij��ѧ��ȤС���ѧ�������ֽ���R���ڳ���ѧ���Ľ������˳����У���С��Ϊ���˽�R�볣����������ͭ�Ľ������˳��������̽�����
���������롿���ǿ��ǵ����Ļ�Ա�ͭǿ�������ֽ����Ļ��˳���������²��룺
����һ��Al��Cu��R��������� ����������R�� Al��Cu��
���������ϡ� R��һ������ɫ�Ľ�������R������Һ��ֻ��+2��R������Һ����ɫ�����������ı�����γ�һ�����ܵ�����Ĥ�����������Ȼ���������������Һ��Ϊ��ɫ��
��ʵ��̽����Ϊ��̽����һ�ֲ���������ס��ҡ�����λͬѧ�ֱ���Բ���һ������������������ʵ�鷽����չ��ʵ��̽����
| ���� | ��Ҫ���� | ��Ҫ���� | ʵ����� |
| ����һ | ��ĥR˿����������뵽����ͭ��Һ�� | R˿���渲����һ���ɫ������ | ����һ (���������������) |
| ����� | ��ĥ��ϸ��ͬ��R˿����˿��ͭ˿���ֱ����Dz��뵽�����ͬ��������������Ҳ��ͬ��ϡ������ | ��R˿����������ݻ�������Һ����ɫ�����ɫ ����˿����������ݽϿ� ��ͭ˿����û�����ݲ��� | ����������� R��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ |
| ������ | | ���������� | ���������� |
��������˼��
�������ֲ����������λͬѧ�����۽��������ֱ�ͬѧ��ʵ��ǰû�д�ĥ��˿������ܻᵼ��ʵ����۴������������ȴ�ĥ��˿���ٽ�����뵽��ͬѧ��ʵ���ù�����Һ�У�һ��ʱ�����Һ����ɫ ������ȷ�ϲ������������������������
A����1���Թܼ���ƿ ��2��CaCO3 + 2HCl=CaCl2 + H2O+ CO2�� E C B�����������롿Al��R��Cu (��Cu��R��Al) ��ʵ��̽������������R+H2SO4=RSO4+H2�� ����˿���뵽RSO4[��RCl2��R(NO3)2]��Һ�С�������˼����dz����ɫ����ȥ
���������������������״����;ȷ�����������ƣ�����ʯ����Ҫ�ɷ���̼��ƣ�����ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��������Щ��Ϣ��д��ѧ����ʽ�����ڶ�����̼���ܶȱȿ���������Ӧѡ�������ſ�����E�����ռ���Ҫ���Ʒ�Ӧ���ʣ���Ҫѡ��װ��C��ͨ������ע�����Ŀ��������Ʒ�Ӧ���ʣ� R��Cu��Al���ֽ�����ԵIJ�����Al��Cu��R��R��Al��Cu��Al��R��Cu�������������R�ܰ�����ͭ�е�ͭ�û���������ʵ��֪��R�Ļ�Ա�ͭǿ���ʲ���һ�Dz������ģ������ڻ�������R�Ļ��ϼ���+2������R��ϡ���ᷴӦ�Ļ�ѧ���ʽ��R+H2SO4=RSO4+H2����ͨ��ǰ���ʵ���Ѿ�֪��Al��R�Ļ�Զ�����ǿ��ͭ�Ļ�Ա�������Ҫ֤��������������ֻ�����ʵ��Ƚ�R��Al�Ļ��ǿ��������ʵ�������֪�ǽ���˿���뵽R������Һ�У����ݲ������ʵ���֪�����Ļ�Ա�Rǿ������������Һ����ɫ�ģ����Խ���ĥ�����˿�ŵ�R������Һ�пɿ�����Һ��ɫ��dz����ɫ����ȥ������

��ϰ��ϵ�д�
�����Ŀ