题目内容
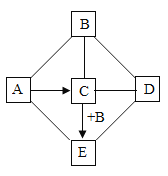
【题目】海水是巨大的资源宝库。如图所示利用海水为原料可获得许多化工产品。
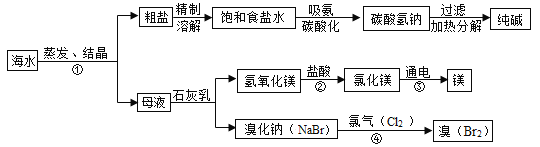
(1)要鉴别海水是硬水还是软水,可选用的试剂是___________________。
(2)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和_______。
(3)粗盐中含有泥沙、MgSO4、CaCl2 等杂质。要提纯粗盐,先将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠: a 过滤; b 加过量的Ba (OH) 2溶液;c 加适量的盐酸;d加过量的Na2CO3溶液; e蒸发。正确的操作顺序是_________________( 填字母 )
(4)步骤②发生反应的化学方程式是___________________。
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),试写出该反应的化学方程式_________; 此反应能够发生是因为_________。
【答案】肥皂水 玻璃棒 bdace(过滤可重复使用) ![]()
![]() 氯气的非金属性比溴的非金属性强或氯气的活动性比溴的活动性强
氯气的非金属性比溴的非金属性强或氯气的活动性比溴的活动性强
【解析】
(1)向海水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此可以用肥皂水鉴别海水是硬水或软水;
(2)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和玻璃棒;
(3)正确的操作顺序是加过量的Ba(OH)2溶液,加过量的Na2CO3溶液,过滤,加适量的盐酸,蒸发,即正确顺序是bdace;
(4)步骤②中,氢氧化镁和稀盐酸反应生成氯化镁和水,发生反应的化学方程式是:Mg(OH)2+2HCl=MgCl2+2H2O;
(5)步骤④中,因为氯气的非金属性比溴的非金属性强,所以溴化钠和氯气反应生成氯化钠和溴,反应的化学方程式为:2NaBr+Cl2=2NaCl+Br2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目