题目内容
【题目】如图为甲、乙两种盐的溶解度曲线,下列说法正确的是
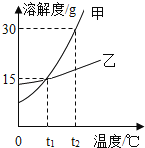
A.甲、乙两种物质的溶解度都不相等
B.将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法
C.t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15%
D.t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克
【答案】B
【解析】A、溶解度大小比较需要指明具体的温度,故A错误;
B、甲的溶解度随温度升高而增大,故甲的不饱和溶液变为饱和溶液需要蒸发或降温,故B正确;
C、t1℃时,甲、乙两种物质的溶解度相同,所以它们的饱和溶液中,溶质的质量分数均为![]() ×100%<15%,故C错误;
×100%<15%,故C错误;
D、t2℃时,乙物质的溶解度小于30g,此温度下,将30克乙物质放入100克水中,所得溶液的质量小于为130克,故D错误;
故选B.

【题目】某兴趣小组同学利用自己设计的实验装置(装置气密性良好)进行了两组实验,研究密闭装置内压强变化的原因(注:NaOH溶液能吸收二氧化碳气体).

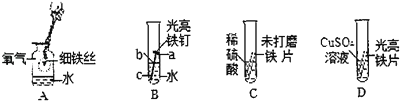
(1)实验一:实验装置如图所示.
实验操作 | 实验现象 | |
① | 将点燃木炭,分别伸入250mL盛有氧气的集气瓶中,迅速塞紧橡皮塞 | |
② | 冷却至室温后,打开止水夹K | A、B均无明显现象 |
③ | 关闭止水夹K,分别将2mL分液漏斗中的溶液滴入集气瓶,一段时间后,打开止水夹K | A中部分水倒吸入集气瓶中,B中水不倒吸 |
④ | 将装置B中的集气瓶放在盛有冰水的水槽中 | B中部分水倒吸入集气瓶中 |
实验分析:步骤③向B中集气瓶内滴加饱和NaHCO3溶液,一段时间后,打开止水夹K,水不倒吸的原因可能是 .
(2)实验二:实验装置如图C所示.若打开止水夹a,关闭止水夹b,在Ⅱ中加入适量澄清石灰水,Ⅰ中加入一种常见固体和一种过量的液体,迅速塞紧橡胶塞,观察到Ⅱ中导管口有气泡冒出,溶液变浑浊.小周同学在观察到Ⅰ中仍有大量气泡产生时,打开止水夹b,关闭止水夹a,此时观察到的实验现象是 .
(3)通过上述实验可以得出,导致密闭装置内压强变化的因素有 (填字母).
A.装置内气体的分子大小 B.装置内的温度 C.装置内气体的分子数目.