题目内容
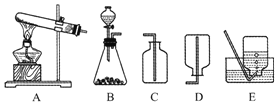
【题目】根据如图所示装置回答下列有关问题:
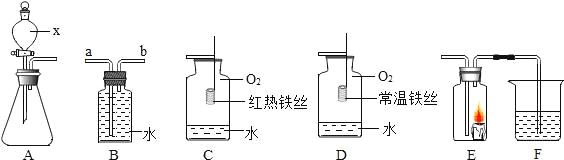
(1)仪器x的名称是_____。
(2)若用装置B收集氧气,进气口应为_____端(选填“a”或“b”)
(3)装置C中水的作用是_____。
(4)对比装置C和D,可以得出关于可燃物燃烧的条件是_____;
(5)某同学连接A、E、F进行实验,A中所加药品不同,F中所加药品相同。
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则E中现象说明A中产生的气体所具有的性质是_____;
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为_____。
【答案】分液漏斗 b 防止集气瓶底炸裂 温度要达到可燃物的着火点 不支持燃烧也不燃烧 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
熟记仪器的名称;根据氧气的密度比水小;铁丝在氧气中燃烧的注意事项;实验中的对比;若实验时E中蜡烛熄灭,F中溶液变浑浊,则E中现象说明A中产生的气体是二氧化碳,它所具有的性质是:不支持燃烧也不燃烧;若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应生成的是氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平。
(1)仪器x是分液漏斗;故填:分液漏斗
(2)氧气不易溶于水且密度比水小,所以用装置B来收集氧气时,氧气从短管进入;故填:b
(3)为了防止高温生成物溅落,炸裂瓶底,在做铁丝在氧气中燃烧实验前要事先在集气瓶内加入少量水或铺一层细沙;故填:防止集气瓶底炸裂
(4)C中红热的铁丝在氧气中能够剧烈燃烧,而D中常温的铁丝在氧气中不燃烧,对比可知燃烧的条件之一是温度要达到可燃物的着火点;故填:温度要达到可燃物的着火点
(5)①若实验时E中蜡烛熄灭,F中溶液变浑浊,则E中现象说明A中产生的气体是二氧化碳,它所具有的性质是:不支持燃烧也不燃烧;故填:不支持燃烧也不燃烧
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应生成的是氧气,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故填:2H2O2![]() 2H2O+O2↑
2H2O+O2↑

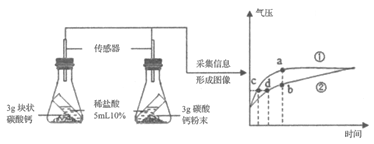
【题目】两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想)
甲同学:A是铁粉,B是二氧化锰.
乙同学:A是炭粉,B是氧化铜.
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是_____. |
②取少量B粉末于试管中,加入适量稀硫酸. | _____,溶液显蓝色. | B粉末是氧化铜. |
(反思与拓展)
(1)将这两种黑色粉末混合加热,观察到黑色粉末逐渐变为红色,澄清石灰水变浑浊.黑色粉末A和B发生反应的化学方程式为_____.
(2)乙同学的猜想正确.
【题目】钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。在实验室,小亮先取定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤被的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(查阅资料)Na2SO4溶液呈中性
(猜想与假设)猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:____________
猜想四:Na2SO4、CuSO4和NaOH
小明认为猜想______不合理,理由是_______(用化学方程式表示)。
(实验与验证)
实验 | 实验操作 | 实验現象 | 实验结论 |
实验一 | 取少量滤液于试管中,仔细观察现象 | 溶液为无色 | 猜想_____不成立 |
实验二 | 向实验一所取滤液中滴入酚酞溶液 | ________ | 猜想二不成立 |
实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想_____成立 |
(拓展延伸)金属活动性顺序表中钠及前面的金属____(填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。