题目内容
【题目】某化学兴趣小组利用以下装置探究气体的制取及性质。结合下图回答有关问题:
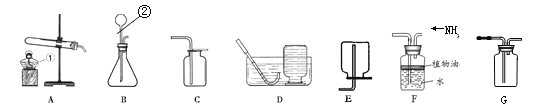
请结合图示实验装置,回答下列问题。
(1)图中标号的仪器名称①___________,②___________。
(2)若选择氯酸钾制取氧气,该反应的符号表达式为________________________,实验中收集的氧气用于完成铁燃烧的实验,则可选用的装置组合是________,实验结束后,应该先_______________,再________________; 若改用装置G收集氧气,氧气应从________端通入(选填“左”或“右”)。
(3)已知NH3极易溶于水且与能水反应,密度比空气小,实验室可用固体氢氧化钙[Ca(OH)2]和氯化铵(NH4Cl)加热来制取NH3,同时生成氯化钙(CaCl2)和水, 该反应的符号表达式为_______________________,若用F装置收集NH3,油层的作用是 ____________________。
(4)萌萌同学通过互联网得知:多种物质都能催化过氧化氢的分解。
【初次探究】实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解,如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后质量和________不变。
【再次探究】CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用。萌萌同学作了以下分析和设计。
①萌萌同学认为最不可能的是H2O,他的理由是 ____________________ 。
②要说明另外的两种粒子是否起到催化作用,萌萌同学设计了如下实验,完成了探究活动。
实验步骤 | 实验现象 | 结论 |
取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是____ |
b. 另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴氯化铜溶液 | 溶液中有大量气泡放出 |
(5)可可同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,该同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想 I:反应生成的锰酸钾分解放出O2;
猜想Ⅱ:_____________________________ ;
猜想Ⅲ:反应生成的锰酸钾和二氧化锰都分解放出O2;
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想______错误;
第二组同学取锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想I正确的结论。该组同学选择的实验方法是________________________。
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快。请说明高锰酸钾在氯酸钾的分解反应中是否作催化剂,为什么?_______________________________________________。
【答案】 酒精灯 长颈漏斗 略 AD 从水中撤出导管 熄灭酒精灯 左 略 防止氨气溶于水,并与水反应而收集不到氨气 化学性质 过氧化氢溶液中含有水 Cu2+ 反应生成的二氧化锰分解放出O2 Ⅱ 实验方法是用带火星的木条伸入试管,若复燃,则猜想Ⅰ正确 高锰酸钾不是催化剂,因为高锰酸钾质量改变
【解析】 (1)根据常见仪器及其名称可知:①是酒精灯,②是长颈漏斗。(2)选择氯酸钾制取氧气,且用于完成铁燃烧的实验,则需在集气瓶底部放少量的水,则可选用的装置组合为:AD。若用装置G收集氧气,因为氧气的密度比空气大,氧气应从左端通入;反应的化学方程式为: ![]()
![]()
![]()
![]() 。(3)实验室可用固体氢氧化钙和氯化铵加热来制取
。(3)实验室可用固体氢氧化钙和氯化铵加热来制取![]() ,反应的化学方程式为;
,反应的化学方程式为; ![]()
![]()
![]() ,已知NH3极易溶于水且与能水反应,密度比空气小,所以采用向上排空气法收集,油层的作用是防止氨气溶于水,并与水反应而收集不到氨气。(4)
,已知NH3极易溶于水且与能水反应,密度比空气小,所以采用向上排空气法收集,油层的作用是防止氨气溶于水,并与水反应而收集不到氨气。(4)![]() 初次探究
初次探究![]() 实验证明,在过氧化氢溶液中滴加
实验证明,在过氧化氢溶液中滴加![]() 溶液能显著加快过氧化氢的分解,如果要确定
溶液能显著加快过氧化氢的分解,如果要确定![]() 是催化剂,还必须通过实验确定它在化学反应前后的化学性质和质量都没有发生改变。
是催化剂,还必须通过实验确定它在化学反应前后的化学性质和质量都没有发生改变。![]() 再次探究
再次探究![]() ①小红同学认为最不可能的是
①小红同学认为最不可能的是![]() ,他的理由是过氧化氢溶液溶液中有水,所以水不是催化剂。 ②完成探究活动如下表所示:
,他的理由是过氧化氢溶液溶液中有水,所以水不是催化剂。 ②完成探究活动如下表所示:
实验步骤 | 实验现象 | 结论 |
a.取一支试管加入 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是铜离子 | b.另取一支试管加入 | 溶液中有大量气泡放出 |
(5)![]() 提出猜想
提出猜想![]() 根据猜想组合可知,猜想Ⅱ:反应生成的二氧化锰分解放出
根据猜想组合可知,猜想Ⅱ:反应生成的二氧化锰分解放出![]() ;
;![]() 实验验证
实验验证![]() 第一组同学取一定质量的二氧化锰,在
第一组同学取一定质量的二氧化锰,在![]() 条件下加热一段时间,冷却后测得
条件下加热一段时间,冷却后测得![]() 的质量不变,则猜想Ⅱ错误;第二组同学取锰酸钾在
的质量不变,则猜想Ⅱ错误;第二组同学取锰酸钾在![]() 条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是把带火星的木条放入试管中,通过观察带火星的木条是否复燃来判断是否产生了氧气。
条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是把带火星的木条放入试管中,通过观察带火星的木条是否复燃来判断是否产生了氧气。![]() 拓展延伸
拓展延伸![]() 高锰酸钾不是氯酸钾分解的催化剂,因为高锰酸钾受热分解生成的二氧化锰是氯酸钾分解的催化剂。
高锰酸钾不是氯酸钾分解的催化剂,因为高锰酸钾受热分解生成的二氧化锰是氯酸钾分解的催化剂。

【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究,请你参与。
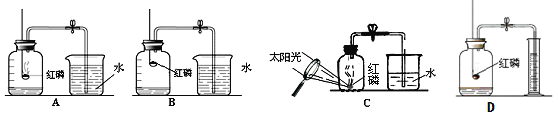
【设计实验】第一小组同学共同设计了如上图的A、B两套装置。 你认为合理的是(填编号)________ 。
【进行实验】
【数据分析】 实验结束后,整理数据如下:(注:集气瓶容积为100ml)
组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入瓶中水的体积(ml) | 20 | 18 | 19 | 17 | 21 | 19 |
通过对实验数据分析,实验得出氧气约占空气体积的___________。
【实验分析】(1)红磷要足量的原因是___________________________;
(2)发生反应的化学方程式是____________________________;
(3)实验结束,发现测定出的空气中氧气的体积分数低于l/5,可能的原因是______
①可能使用红磷的量不足,瓶内氧气没有消耗完
②可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
③可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
④可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
【改进实验】
(1)第二小组同学设计了C实验装置,优点是:________________________________。
(2)第三小组同学设计了D实验装置,优点是:_______________________________。