��Ŀ����
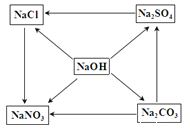
����Ŀ���ס��ҡ����dz��г��������ʣ�������H��C��O��Cl��Ca����Ԫ���е�һ�ֻ�����ɡ�����֮��Ĺ�ϵ��ͼ��ʾ��ͼ����������ʾ���ʼ���ڵ�ת����ϵ�����ַ�Ӧ������P��Ӧ����������ȥ��
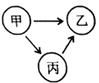
��1�����ס������Ԫ����ͬ��������ʵ������ȡ����������___________������Ҫ��;��_____________________________________________��дһ�㣩��
��2�����ҡ������Ԫ����ͬ������һ�ֺ�ɫ���壬�����º��ȶ�����ת�����ҵĻ�ѧ����ʽ___
��
��3�����ס��ҡ��������н���Ԫ�أ�������������������������ת��Ϊ�ҵĻ�ѧ����ʽ_______��
���𰸡�O2�������� ֧��ȼ�ջ����� 2CO+O2![]() 2CO2��2CO2+C
2CO2��2CO2+C![]() 2CO CaO+2HCl=CaCl2+H2O+CO2��
2CO CaO+2HCl=CaCl2+H2O+CO2��
��������
��1�����ס������Ԫ����ͬ��������ʵ������ȡ������ˮ������������Ԫ����ͬ�����й��������ڶ������̴������·ֽ�����ˮ��������������������ȡ���������Ϊ�������⣬��Ϊ��������������ܲ����ң����������ڶ������̴������·ֽ�����ˮ��������ˮͨ���ֽܷ����������������������O2��������������Ҫ��;��֧��ȼ�ջ�������
��2������һ�ֺ�ɫ���壬�����º��ȶ����������̼���ҡ������Ԫ����ͬ������ת��Ϊ�ҡ�����̼����������ȫȼ�����ɶ�����̼������ȫȼ������һ����̼����ת�����ң�������̼�ڸ��������·�Ӧ����һ����̼��һ����̼��������ȼ�����ɶ�����̼������Ƕ�����̼����һ����̼��������һ����̼���������̼������ת�����ҵķ��ǻ�ѧ����ʽ��2CO+O2![]() 2CO2��2CO2+C
2CO2��2CO2+C![]() 2CO��
2CO��
��3���������������������������Ϊ�������ƣ��ס��ҡ��������н���Ԫ�أ�����ת��Ϊ�����ң���������ˮ�����������ƣ������������ᷴӦ�����Ȼ��ƺ�ˮ���������������ᷴӦ�����Ȼ��ƣ����������ƣ���Ϊ�Ȼ��ơ���ת��Ϊ�ҵĻ�ѧ����ʽΪ��CaO+2HCl=CaCl2+H2O+CO2����

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�����Ŀ����ͳ�ƣ��ҹ�ÿ�걨�ϵ��ֻ�����1�ڲ�������������Ч�������ã�����ɾ���˷Ѻ���Ⱦ��ͬѧ�ǶԷϾ��ֻ��еĽ������ղ�����Ȥ��
��������⣩
�ӷϾ��ֻ��п��Ի��յ���Щ�м�ֵ�Ľ�������λ��գ�

���������ϣ�
�����ֻ���·���еĽ�������۸����±���ʾ��
���� | Fe | Cu | Al | Ni | Au | Ag | Pd���٣� |
�г��۸�/��$/t�� | 365 | 7175.5 | 1710.5 | 14235 | 4.7��107 | 7.6��105 | 2.7��107 |
��ʯ�к��� | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
�ֻ���·���к��� | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
˵����Fe��Cu��Al��Ni�ĺ���������������%����ʾ��Au��Ag��Pd�ĺ����ĵ�λΪ��g/t����
��Ni�Ľ������λ����ǰ��Pd�Ľ������λ�����NiCl2��ҺΪ��ɫ��
��ʵ�鷽����

��һ����ѡ��ֵ�û��յĽ�����
�������Ϣ��е����ݣ��Ͼ��ֻ����л��ռ�ֵ�Ľ�����Au��Ag��Cu��Pd��
��1��ԭ���ǣ������ǵ��г��۸�ϸߣ���_____��
�ڶ��������ʵ����롢���ղ��ֽ�����
��� | ʵ�鲽�� | ʵ������ |
�� | ȡһ�Ͼ��ֻ���·�壬�õ紵���������·���ӵ�ĺ������ȷ磬һ��ʱ��������ӽ�������·�����ϰ���ק�� | �����ۻ� |
�� | ��������·�����ձ��У��������10%��ϡ������� | ���� |
�� | ȡ����δ�ܽ�Ľ�����·��������ˮϴ����������ͼ��ʾװ���У�����ʵ�顣 | ��Һ�����ɫ����������������δ�ܽ� |
�� | ���ˢ����ձ��е����ʣ�ϴ����ֽ�ϵ����� | ��ֽ���������������� |
���������ۣ�
��2���ɲ���I�е�������֪�ĺ���������������_____������ĸ����
a.�۵�� b.Ӳ�ȴ� c.����ʴ��ǿ
��3���������ʵ������������������Ϊ37%���ܶ���1.18gmL-1��Ũ��������10%������185g����ҪŨ����_____ml�����Ƹ�ϡ����Ӧѡ�����Ͳ���̣�ˮ���ܶ�Ϊ1g/cm3��Ϊ_____������ĸ����
a.10ml b.50ml c.100ml d.200ml
��4�������������Һ�У����ٺ���_____�������֣������ʣ��ò����ж�Ӧ��ʵ��������_____��
��5����д��������У���Һ�����ɫ�Ļ�ѧ����ʽ_____��
��6��������й��˲����õ��IJ��������в�������_____��_____�����в�������������_____��